题目内容
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 0.1 mol/L NaAlO2溶液中:H+、Na+、Cl-、SO3- | |
| B. | 无色溶液中:K+、Ca2+、Cl-、NO3- | |
| C. | 使酚酞变红色的溶液中:Na+、Cu2+、HCO3-、NO3- | |
| D. | 使石蕊变红的溶液中:H+、Na+、Fe2+、MnO4- |
分析 A.氢离子与亚硫酸根离子、偏铝酸根离子反应;
B.四种离子之间不反应,且都是无色离子;
C.使酚酞变红色的溶液为碱性溶液,铜离子与碳酸氢根离子发生双水解反应,且铜离子和碳酸氢根离子都与氢氧根离子反应;
D.使石蕊变红的溶液中存在大量氢离子,酸性高锰酸根离子具有强氧化性,能够氧化亚铁离子.
解答 解:A.H+与AlO2-、SO3-反应,在溶液中不能大量共存,故A错误;
B.K+、Ca2+、Cl-、NO3-之间不发生反应,都是无色离子,在溶液中能够大量共存,故B正确;
C.使酚酞变红色的溶液中存在大量氢氧根离子,Cu2+、HCO3-之间发生反应,且二者都与氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.H+、Fe2+、MnO4-之间发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
7.亚氯酸钠(NaClO2)是一种性能优良的漂白剂,但在酸性溶液发生分解:5HClO2→4ClO2↑+H++Cl-+2H2O.向亚氯酸钠溶液中加入盐酸,反应剧烈.若将盐酸改为pH相同的稀硫酸,开始反应缓慢,稍后产生气体速度较快,速度变化的原因是( )
| A. | 逸出ClO2使生成物浓度降低 | B. | 酸使HClO2的分解加速 | ||
| C. | 溶液中的H+起催化作用 | D. | 溶液中的Cl-起催化作用 |
11.下列关于如图所示电化学装置的分析正确的是( )
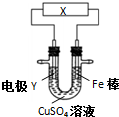

| A. | 若X为直流电源,Y为铜棒接正极,则Fe棒上镀铜 | |
| B. | 若X为直流电源,Y为碳棒接负极,则Fe棒被保护 | |
| C. | 若X为电流计,Y为锌棒,则SO42- 移向Fe棒 | |
| D. | 若X为导线,Y为铜棒,则Fe棒发生还原反应 |
5.下列有关实验装置进行的相应实验,能达到实验目的是( )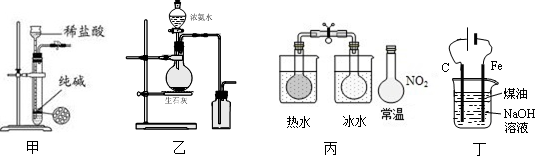

| A. | 用图甲所示装置控制制取少量纯净的CO2气体 | |
| B. | 用图乙所示装置制取并收集氨气 | |
| C. | 用图丙所示装置可以说明反应2NO2(g)?N2O4(g)是放热反应 | |
| D. | 用图丁所示装置可制备Fe(OH)2并能较长时间观察其颜色 |
6.下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
| A. | 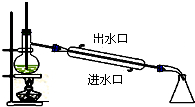 石油的蒸馏 | B. | 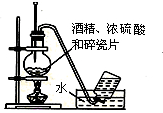 实验室用乙醇制乙烯 | ||
| C. | 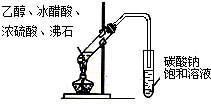 实验室制取乙酸乙酯 | D. | 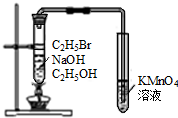 验证溴乙烷发生消去反应 |
 CO2
CO2

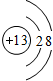 Cl
Cl .
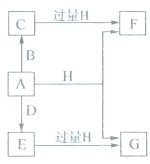
.
 .
.
 .
.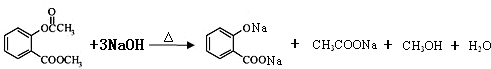 .
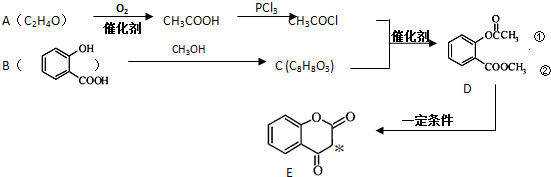
.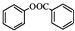 ),根据题目信息设计合成线路,请写出最后一步反应的化学方程式:
),根据题目信息设计合成线路,请写出最后一步反应的化学方程式: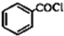 +
+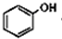 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$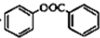 +HCl.
+HCl.