题目内容
12.S02是常见的大气污染物,燃煤是产生S02的主要原因.工业上有多种方法可以减少S02的排放.
(1)往煤中添加一些石灰石,可使燃煤过程中产生的S02转化成硫酸钙.该反应的总化学方程式是2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2.
(2)可用多种溶液做燃煤烟气中SO2的吸收液.
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHS03时,两种吸收液体积比V(Na2SO3):V(NaOH)=1:2
②NaOH溶液吸收了足量的:SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式是Ca2++OH-+HSO3-=CaSO3↓+H2O.
(3)甲同学认为BaCl2溶液可以做SO2的吸收液.为此甲同学设计如下实验(夹持装置和加热装置略如图1,气密性已检验).反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B中有白色沉淀.甲同学认为B中白色沉淀是SO2与BaCl2溶液反应生成的BaSO3,所以BaCl2溶液可做SO2吸收液.
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是:
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCI2溶液反应生成BaSO4沉淀.
②为证明SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略如图2,气密性已检验):
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其它现象;D中红色褪去.
③试管B中试剂是饱和NaHSO3溶液;滴加浓硫酸之前的操作是打开弹簧夹,通入N2,一段时间后关闭弹簧夹
④通过甲、乙两位同学的实验,得出的结论是SO2与BaCl2溶液不能得到BaSO3沉淀;不能用BaCl2溶液做吸收SO2的吸收液.
分析 (1)根据反应物、生成物和反应条件书写化学方程式;
(2)①根据Na2SO3+SO2+H2O═2NaHSO3,NaOH+SO2═NaHSO3分析解答;
②NaOH溶液吸收了足量的SO2后生成NaHSO3,与一定量的石灰水溶液充分反应生成亚硫酸钙、氢氧化钠、水;
(3)二氧化硫具有还原性易被氧气氧化成三氧化硫,三氧化硫与水反应生成硫酸,与BaCl2溶液反应生成BaSO4沉淀;
③为证明SO2与BaCl2溶液不能得到BaSO3沉淀,可通入氮气排出装置中的氧气;④通过甲乙两位同学的实验现象进行对比分析.
解答 解:(1)根据题意,碳酸钙与二氧化硫、氧气在高温条件下反应生成硫酸钙,同时生成二氧化碳,所以反应的方程式为:2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2,
故答案为:2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2;
(2)①假设生成的NaHSO3物质的量都为2mol,Na2SO3+SO2+H2O═2NaHSO3,吸收的二氧化硫的物质的量为2mol,需1molNa2SO3,NaOH+SO2═NaHSO3,吸收的二氧化硫的物质的量也为2mol,需2molNaOH,假设Na2SO3溶液和NaOH溶液的物质的量浓度都为cmol/L,两种吸收液体积比V(Na2SO3):V(NaOH)=$\frac{1}{c}$:$\frac{2}{c}$=1:2,
故答案为:1:2;
②NaOH溶液吸收了足量的SO2发生反应:NaOH+SO2═NaHSO3,与一定量的石灰水溶液充分反应NaHSO3+Ca(OH)2=CaSO3↓+NaOH+H2O,离子反应为:Ca2++OH-+HSO3-=CaSO3↓+H2O,使NaOH溶液再生,
故答案为:Ca2++OH-+HSO3-=CaSO3↓+H2O;
(3)二氧化硫具有还原性易被氧气氧化成三氧化硫,与BaCl2溶液反应,三氧化硫与水反应生成硫酸,H2SO4+BaCl2=BaSO4↓+2HCl,
故答案为:A中产生的SO2与装置内空气中的O2进入B中与BaCl2溶液反应生成BaSO4沉淀;
③滴加浓硫酸之前打开弹簧夹,通入N2,排出装置中的氧气,然后滴加浓硫酸,Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,A中产生的白雾是浓硫酸的酸雾,所以B中的试剂是饱和NaHSO3,除去白雾,
故答案为:饱和NaHSO3;打开弹簧夹,通入N2,一段时间后关闭弹簧夹;
④通过甲乙两位同学的实验,得出的结论是SO2与BaCl2溶液不能得到BaSO3沉淀;不能用BaCl2溶液做吸收SO2的吸收液,
故答案为:SO2与BaCl2溶液不能得到BaSO3沉淀;不能用BaCl2溶液做吸收SO2的吸收液.
点评 本题考查了二氧化硫性质的实验验证分析判断,题目难度中等,掌握物质性质的分析、装置特征的判断及反应条件的应用方法是解题关键,试题知识点较多、综合性较强,充分考查了学生的分析能力及化学实验能力.

| A. | 3-甲基丁醛 (CH3)2CHCH2COH | B. | TNT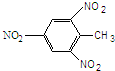 | ||
| C. | 硬脂酸甘油酯 | D. | 乙酸甲酯 CH3OOCCH3 |
| A. | CH3COOH的电离平衡常数增大为原来的10倍 | |
| B. | CH3COO-与CH3COOH的浓度之比增大为原来的10倍 | |
| C. | CH3COOH与CH3COO-的浓度之和减小为原来的$\frac{1}{10}$ | |
| D. | CH3COO-与H+的浓度之积减小为原来的$\frac{1}{10}$ |
| A. | 2.4 g金属镁所含电子数目为0.2 NA | |
| B. | 标准状况下22.4L CH4所含原子数目为NA | |
| C. | 17 g NH3 所含质子数目为10 NA | |
| D. | 物质的量浓度为1mol/L的MgCl2溶液中,含有Cl-个数为2NA |
在温度T1和T2时,分别将0.50molCH4和1.2molNO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A. | 10 min内,T1时υ(CO2)比T2时小 | B. | 温度:T1>T2 | ||
| C. | a<0 | D. | 平衡常数:K(T1)<K(T2) |
| A. | 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 | |
| B. | 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 | |
| C. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 | |
| D. | 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
| A. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 铁溶于过量稀硝酸中:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| C. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O | |
| D. | 醋酸溶液与NaHCO3溶液反应:H++HCO3-═CO2↑+H2O |