题目内容
4.向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO+H2O(g)$?_{高温}^{催化剂}$CO2+H2.当反应达到平衡时,CO的体积分数为x.若维持容器的体积和温度不变,超始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )| A. | 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 | |
| B. | 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 | |
| C. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 | |
| D. | 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
分析 恒温恒容下,该反应前后气体体积不发生变化,将物质全部转化到左边满足n(CO):n(H2O)=1:2,为等效平衡,平衡时CO的体积分数相同,不同配比达到平衡时CO的体积分数大于原平衡中CO的体积分数x,说明不同配比全部转化到左边应n(CO):n(H2O)>1:2,据此进行解答.
解答 解:恒温恒容下,该反应前后气体体积不发生变化,将物质全部转化到左边满足n(CO):n(H2O)=1:2,为等效平衡,平衡时CO的体积分数相同,不同配比达到平衡时CO的体积分数大于原平衡中CO的体积分数x,说明不同配比全部转化到左边应n(CO):n(H2O)>1:2,
A.0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2等效为1.5 molCO+3 molH2O(g),n(CO):n(H2O)=1:2,平衡时CO的体积分数为x,故A错误;
B.1mol CO+1mol H2O(g)+1mol CO2+1mol H2等效为2 molCO+2 molH2O(g),n(CO):n(H2O)=1:1>1:2,平衡时CO的体积分数大于x,故B正确;
C.0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4molH2等效为0.9 molCO+1.9 molH2O(g),n(CO):n(H2O)=9:19<1:2,平衡时CO的体积分数小于x,故C错误;
D.0.5mol CO+1.5mol H2O(g)+0.5molCO2+0.5mol H2等效为1 molCO+2 molH2O(g),n(CO):n(H2O)=1:2,平衡时CO的体积分数等于x,故D错误;
故选B.
点评 本题考查了化学平衡的影响因素分析、等效平衡的应用判断,题目难度中等,极值转化是解题的关键,注意掌握等效平衡的判断方法,试题培养了学生的分析能力及灵活应用能力.

 阅读快车系列答案
阅读快车系列答案| A. | 18g H2O所含的电子数目为9NA | |
| B. | 0.1mol/L Na2SO4溶液所含Na+数目为0.2NA | |
| C. | 标准状况下22.4 LO2所含的原子数目为NA | |
| D. | 1mol Na完全反应时所失去的电子数为NA |
| A. | 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O | |
| C. | 惰性电极电解MgCl2溶液:Cl-+2H2O═2OH-+H2↑+Cl2↑ | |
| D. | 次氯酸钙溶液中通入少量的二氧化碳:2ClO-+CO2+H2O═CO32-+2HClO |
| A. | 用蒸发皿进行加热蒸发时,不需要垫加石棉网即可直接进行加热 | |
| B. | 蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,以防止液体发生局部过热而暴沸 | |
| C. | 蒸馏时,冷凝水应从冷凝管上口进,下口出 | |
| D. | 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
| A. | 标准状况下,22.4 L 14CO2与44 g 14CO2含分子数均为NA | |
| B. | 1 mol CH3COOH与足量CH3CH2OH在浓硫酸存在下共热生成NA个乙酸乙酯分子 | |
| C. | 常温下,pH=13的NaOH溶液中含OH-离子数为0.1 NA | |
| D. | 浓度为2 mol/L的FeCl3溶液500 mL水解后生成Fe(OH)3胶体粒子数目小于NA |

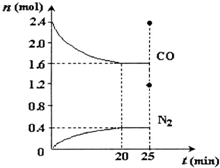 对含氮物质的研究和利用有着极为重要的意义.
对含氮物质的研究和利用有着极为重要的意义.