题目内容
【题目】25℃时,pH=2 的盐酸和醋酸溶液各 1 mL 分别加水稀释,pH 随溶液体积变化的曲线如图所示。下列说法正确的是
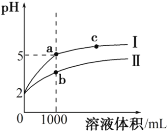
A.曲线 I 代表醋酸溶液的稀释过程
B.a 溶液的导电性比 c 溶液的导电性差
C.将 a、b 两溶液加热至 30℃(忽略溶质挥发),![]() 变大
变大
D.与相同浓度的NaOH 溶液恰好中和时,消耗a 溶液的体积比 b 溶液的体积大
【答案】D
【解析】
A.1 mL pH=2的盐酸加水稀释至1000 mL,溶液的pH=5;1 mL pH=2的醋酸加水稀释至1000 mL ,CH3COOH的电离平衡正向移动,溶液的pH<5,故曲线I代表盐酸的稀释过程,曲线II代表醋酸的稀释过程,故A错误;
B.盐酸加水稀释时,溶液中c(Cl-)、c(H+)减小,溶液的导电能力减弱,故a点溶液的导电性比c点溶液的导电性强,故B错误;
C.升高温度,CH3COOH的电离平衡正向移动,c(CH3COO-)增大,而c(Cl-)基本不变,所以![]() 变小,故C错误;
变小,故C错误;
D.pH=2的盐酸和醋酸相比,c(CH3COOH)>c(HCl),体积相等的两种溶液中n(CH3COOH)>n(HCl),与NaOH溶液发生中和反应时,CH3COOH消耗NaOH多,故消耗a 溶液的体积比 b 溶液的体积大,故D正确;
故答案为D。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案【题目】在![]() 密闭容器内,800℃时在反应
密闭容器内,800℃时在反应![]() 体系中,
体系中,![]() 随时间的变化如表所示:
随时间的变化如表所示:
时间/ | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
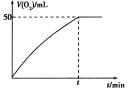
(1)下图表示![]() 的变化的曲线是________。用
的变化的曲线是________。用![]() 表示
表示![]() 内该反应的平均速率
内该反应的平均速率![]() ________。
________。
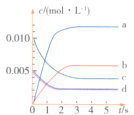
(2)能说明该反应已达到平衡状态的有________(填序号,下同)。
a ![]() b 容器内压强保持不变
b 容器内压强保持不变
c ![]() d 容器内密度保持不变
d 容器内密度保持不变
(3)为使该反应的反应速率增大,下列措施正确的有________。
a 适当升高温度 b 增大![]() 的浓度 c 选择高效催化剂解粉
的浓度 c 选择高效催化剂解粉