题目内容
【题目】某小组同学在实验室中组装如下图所示装置,请回答:
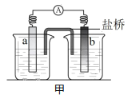
(1)从能量转化的角度看,该装置是将____(填能量转化的形式),符合该装置的化学反应类型一定是____反应。
(2)若 a 为锌片,b 为铜片,左右两侧烧杯中分别盛有ZnSO4溶液和CuSO4 溶液,则 b 极的电极反应式是_____,a 极可观察到的现象是______;导线中电子流动的 方向是_____(用“a→b”或“b→a”表示),盐桥中的阳离子向______(填“a”或“b”) 极方向移动。
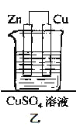
(3)另一种原电池乙如下图所示装置,甲、乙两种原电池中可更有效地将化学能转化为电能的是______(填“甲”或“乙”),其原因是_____。
【答案】化学能转化电能 氧化还原 Cu2++2e-=Cu 锌片溶解 a→b b 甲 电池乙负极可与CuSO4溶液直接发生反应,导致部分化学能转化为热能,电池甲的负极不与所接触的电解质溶液反应,化学能在转化为电能时损耗较小
【解析】
由原电池工作原理,一般活泼金属作负极失去电子发生氧化反应,原电池中电子由负极移向正极,阳离子向正极移动,阴离子向负极移动,据此分析解答。
(1)由图甲装置分析可知,甲为原电池,装置中发生氧化还原反应,有电子的转移,从而将化学能转化为电能,故答案为:化学能转化为电能;氧化还原;
(2)若a为锌片,b为铜片,左右两侧烧杯中分别盛有ZnSO4溶液和CuSO4 溶液,则a作负极,Zn失去电子发生氧化反应,电极反应式为Zn-2e-=Zn2+,因此a极锌片溶解,b作正极,Cu2+在正极得到电子发生还原反应,电极反应式为Cu2++2e-=Cu,原电池中电子由负极移向正极,阳离子向正极移动,则导线中的电子流动的方向是a→b,盐桥中的阳离子向b极方向移动,故答案为:Cu2++2e-=Cu;锌片溶解;a→b;b;
(3)由于带有盐桥的甲原电池中负极没有和CuSO4溶液直接接触,二者不会直接发生置换反应,化学能不会转化为热能,几乎全部转化为电能;而原电池乙中的负极与CuSO4溶液直接接触,两者会发生置换反应,部分化学能转化为热能,化学能不可能全部转化为电能,因此甲、乙两种原电池中可更有效地将化学能转化为电能的是甲,故答案为:甲;电池乙负极可与CuSO4溶液直接发生反应,导致部分化学能转化为热能,电池甲的负极不与所接触的电解质溶液反应,化学能在转化为电能时损耗较小。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c