题目内容
【题目】在![]() 密闭容器内,800℃时在反应
密闭容器内,800℃时在反应![]() 体系中,
体系中,![]() 随时间的变化如表所示:
随时间的变化如表所示:
时间/ | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
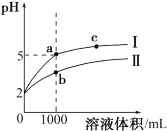
(1)下图表示![]() 的变化的曲线是________。用
的变化的曲线是________。用![]() 表示
表示![]() 内该反应的平均速率
内该反应的平均速率![]() ________。
________。

(2)能说明该反应已达到平衡状态的有________(填序号,下同)。
a ![]() b 容器内压强保持不变
b 容器内压强保持不变
c ![]() d 容器内密度保持不变
d 容器内密度保持不变
(3)为使该反应的反应速率增大,下列措施正确的有________。
a 适当升高温度 b 增大![]() 的浓度 c 选择高效催化剂解粉
的浓度 c 选择高效催化剂解粉
【答案】b ![]() bc abc
bc abc
【解析】
(1)![]() 的起始浓度为
的起始浓度为![]() ,
,![]() 时,
时,![]() 可根据表中
可根据表中![]() 的变化量求解,
的变化量求解,![]()
![]() ,故选b;由表可求
,故选b;由表可求![]() 内,
内,![]()
![]() ,故
,故![]() ,故答案为:b;
,故答案为:b;![]() ;
;
(2)a项,在任意状态下,都存在![]() ,错误;
,错误;
b项,因该反应为反应前后气体体积不等的反应,恒容条件下,压强不变可作为反应达到平衡状态的标志;
c项,由![]() ,可推出
,可推出![]() ,说明反应已达到平衡状态;
,说明反应已达到平衡状态;
d项,由于平衡体系中全是气体,容器体积固定,故任意状态下容器内气体密度不变,错误;故答案为:bc;
(3)a.适当升高温度,反应速率增大,a项正确;
b.增大![]() 的浓度能增大反应速率,b项正确;
的浓度能增大反应速率,b项正确;
c.催化剂能增大反应速率,c项正确;故答案为abc。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】已知:N2(g)+3H2(g)===2NH3(g) △H=-92kJ/mol。起始反应物为![]() 和
和![]() ,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中
,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中![]() 的物质的量分数如下表:
的物质的量分数如下表:
温度 压强 | 400℃ | 450℃ | 500℃ | 600℃ |
20MPa | 0.387 | 0.274 | 0.189 | 0.088 |
30MPa | 0.478 | 0.359 | 0.260 | 0.129 |
下列说法正确的是
A. 体系中![]() 的物质的量分数越大,则正反应速率越大
的物质的量分数越大,则正反应速率越大
B. 反应达到平衡时, ![]() 和
和![]() 的转化率均为1
的转化率均为1
C. 反应达到平衡时,放出的热量均为92.4kJ
D. 600℃,30MPa下反应达到平衡时,生成![]() 的物质的量最多
的物质的量最多