题目内容
14.硫代硫酸钠俗称“海波”,又名“大苏打”,溶液具有弱碱性和较强的还原性,是棉织物漂白后的脱氯剂,定量分析中的还原剂.硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得,装置如图(a)所示.已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如图(b)所示,
(1)Na2S2O3•5H2O的制备:
步骤1:如图连接好装置后,检查A、C装置气密性的操作是关闭K2打开K1,在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶.
步骤2:加入药品,打开K1、关闭K2,加热.装置B、D中的药品可选用下列物质中的ACD.(填编号)
A. NaOH溶液 B.浓H2SO4C.酸性KMnO4溶液 D.饱和NaHCO3溶液
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近或不小于7时,打开K2、关闭K1并停止加热;C中溶液要控制pH的原因是硫代硫酸钠在酸性溶液中不稳定.
步骤4:过滤C中的混合液,将滤液经过加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品.
(2)Na2 S2O3性质的检验:
向足量的新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,检查反应后溶液中含有硫酸根,写出该反应的化学方程式Na2 S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl,
(3)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解.此时CrO2-4全部转化为Cr2O2-7;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.010mol•L-1的Na2S2O3溶液进行滴定,反应完全时,消耗Na2S2O3溶液18.00mL.部分反应的离子方程式为:
Cr2O72-+6I-+14H+=3I2+2Cr3++3I2+7H2O
I2+2S2O32-=S4O62-+2I-
则该废水中Ba2+的物质的量浓度为0.0024mol/L.
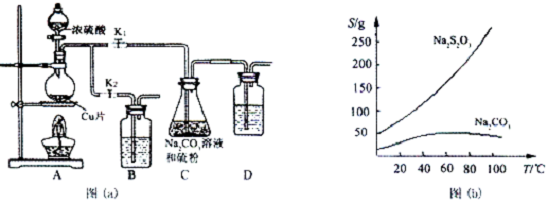
分析 (1)步骤1:利用气体热胀冷缩性质,检验装置气密性;
步骤2:装置B、D的作用是进行尾气处理,防止尾气中二氧化硫污染空气;
步骤3:硫代硫酸钠在酸性溶液中不稳定,应控制溶液为弱碱性,即控制溶液pH接近或不小于7;
步骤4:从溶液中获得晶体,需要加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品;
(2)由题目信息可知,Na2S2O3被氯水氧化反应生成Na2SO4、H2SO4,氯气被还原为HCl;
(3)由题意可知,BaCrO4用盐酸溶解转化为Cr2O2-7,由元素守恒及已知方程式可得关系式:2Ba2+~2BaCrO4~Cr2O2-7~3I2~6Na2S2O3,结合消耗的Na2S2O3利用关系式计算溶液中n(Ba2+),进而计算c(Ba2+).
解答 解:(1)步骤1:利用气体热胀冷缩性质,检验装置气密性,具体操作为:故答案为:关闭K2打开K1,在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶,D中导管有气泡冒出,冷却后形成1段水柱,说明气密性良好,
步骤2:装置B、D的作用是进行尾气处理,防止尾气中二氧化硫污染空气,二氧化硫具有还原性,可以用酸性高锰酸钾溶液氧化吸收,二氧化硫能与氢氧化钠溶液、碳酸氢钠溶液反应被吸收,故选:ACD;
步骤3:硫代硫酸钠在酸性溶液中不稳定,应控制溶液为弱碱性,可以控制溶液pH接近或不小于7,
步骤4:从溶液中获得晶体,需要加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品,
故答案为:关闭K2打开K1,在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶;ACD;pH接近或不小于7;硫代硫酸钠在酸性溶液中不稳定;冷却结晶、洗涤;
(2)由题目信息可知,Na2S2O3被氯水氧化反应生成Na2SO4、H2SO4,氯气被还原为HCl,反应方程式为:Na2 S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl,
故答案为:Na2 S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl;
(3)由题意可知,BaCrO4用盐酸溶解转化为Cr2O2-7,由元素守恒及已知方程式可得关系式:2Ba2+~2BaCrO4~Cr2O2-7~3I2~6Na2S2O3,消耗的Na2S2O3为0.018L×0.01mol/L,则n(Ba2+)=0.018L×0.01mol/L×$\frac{1}{3}$=0.00006mol,故溶液中c(Ba2+)=$\frac{0.00006mol}{0.025L}$=0.0024mol/L,
故答案为:0.0024mol/L.
点评 本题考查实验制备方案设计,涉及气密性检验、对实验装置及步骤的分析评价、物质的分离提纯、氧化还原反应滴定,(3)中注意利用关系式进行计算,难度中等.

| A. | 2.8mol/L | B. | 3.0mol/L | C. | 3.2mol/L | D. | 3.6mol/L |
 ,打破1mol P-Cl键吸收b kJ的热量,打破1mol Cl-Cl键吸收c kJ的热量.下列叙述正确的是( )
,打破1mol P-Cl键吸收b kJ的热量,打破1mol Cl-Cl键吸收c kJ的热量.下列叙述正确的是( )| A. | 1 mol P4(g)和1 mol Cl2(g)所具有的能量和大于1 mol PCl3(g) 所具有的能量 | |
| B. | 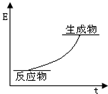 该反应的能量图象可表示 该反应的能量图象可表示 | |
| C. | 形成1mol P-P键放出-($\frac{a}{6}$-2b+c) kJ的热量 | |
| D. | 因为该反应为放热反应,故不需要任何条件就能快速进行 |
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH⑤

| A. | ①③④ | B. | ②④ | C. | ①③⑤ | D. | ①②③⑤ |
| A. | 石油裂解的主要目的是提高汽油等轻质油的产量与质量,石油催化裂化的主要目的是得到更多的乙烯、丙烯等气态短链烃 | |
| B. | 分子式为C3H7C1的有机物有三种同分异构体 | |
| C. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 | |
| D. | 向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
| A. | 气态氢化物的稳定性:D>W | |
| B. | 四种元素一定属于短周期元素 | |
| C. | 最高价氧化物对应水化物的碱性:L>K | |
| D. | 原子序数:L>K>W>D |
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738kJ•mol-1 I2=1 451kJ•mol-1 I3=7 733kJ•mol-1 I4=10 540kJ•mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
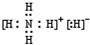 .
.(2)B元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为

该同学所画的电子排布图违背了泡利原理.
(4)G位于ⅦB族d区,该元素的核外电子排布式为[Ar]3d54s2.
(5)检验F元素的方法是焰色反应,请用原子结构的知识解释产生此现象的原因:当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量.
| A. | 随着原子序数的递增,第三周期元素的电负性逐渐减小 | |
| B. | 铝的第一电离能比镁的第一电离能大 | |
| C. | K、Na、Li的第一电离能逐渐增大 | |
| D. | 电负性差值大的元素原子之间形成的化学键主要是共价键 |