【题目】硝酸是一种重要的化工原料,工业上生产硝酸的主要过程中:(1)反应N2(g)+3H2(g) 2NH3(g)△H<0 ;恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡下列图像能正确表示该过程中相关量的变化的是__________。(选填字母)。
2NH3(g)△H<0 ;恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡下列图像能正确表示该过程中相关量的变化的是__________。(选填字母)。

(2)一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的7/10,则N2的转化率a1=________;
若向该容器中再加入1molN2和3molH2,达到平衡状态时,N2的转化率为a2,则a2________a1(填“>”、“<”或“=”)。
(3)2NO(g)+O2(g) 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。

①比较P1、P2的大小关系:P1____P2(填“>”、“<”或“=”)。
②随温度升高,该反应平衡常数变化的趋势是__________。
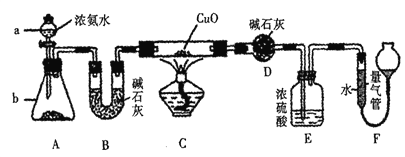
(4)硝酸厂常用如下2种方法处理尾气。
①催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是________________________________。
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。若每4.6gNO2和Na2CO3溶液反应时转移电子数为0.05mol,则反应的离子方程式是___________________________________________。