题目内容
【题目】某课外活动小组欲利用CuO与氨反应,研究氨的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
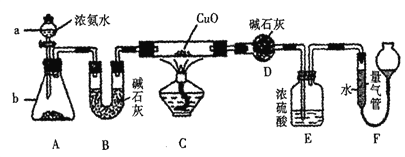
(1)仪器a的名称为 _________。
(2)实验室中,利用装置A,还可制取的无色气体是_________(填字母)。
A.Cl2 B.04 C.C02 D.N02
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管内有无色无味的气体生成,上述现象证明氨气具有________性,写出相应的化学方程式 __________。
(4) D装置的作用是 __________。
(5) E装置中浓硫酸的作用是__________。
(6)读取气体体积前,应对装置F进行的操作是__________。
【答案】 分液漏斗 BC 还原 3CuO+2NH3=3Cu+3H2O+N2 吸收反应生成的水 吸收未反应的氨气,阻止F中水蒸气进入D 慢慢上下移动右边漏斗,使左右两管液面相平
【解析】(1)装置中仪器a为分液漏斗;仪器b是利用分液漏斗中滴入的氨水使锥形瓶中的固体溶解放热促进一水合氨分解生成氨气,氢氧化钠固体、氧化钙固体、碱石灰固体;
(2)利用装置A,可制取的无色气体;A.制备氯气Cl2需要加热,且氯气为黄绿色气体,故A错误;B.可以制备O2,利用固体过氧化钠和水的反应,故B正确;C.可以制备CO2 气体,利用稀盐酸滴入大理石上反应生成,故C正确;D.NO2是红棕色气体,故D错误;故答案为BC;
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,说明氨气和氧化铜反应生成铜和氮气与水,氨气被氧化铜氧化表现还原性,结合原子守恒配平写出的化学方程式为:3CuO+2NH3![]() 3Cu+3H2O+N2 ;
3Cu+3H2O+N2 ;
(4)D装置中的碱石灰是吸收未反应的氨气,阻止F中水蒸气进入D;
(5)依据流程分析,浓硫酸是吸收过量的氨气,阻止F中水蒸气进入D影响实验效果;
(6)读取气体体积前,应对装置F进行的操作是慢慢上下移动右边漏斗,使左右两管液面相平,保持压强平衡再读数。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案