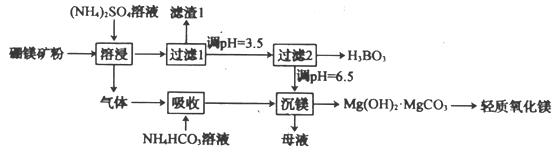
题目内容
【题目】硫酸镍(NiSO4)是一种重要的化工原料,广泛应用于电镀、医药、印染等工业。以含镍废催化剂(主要含Ni及少量的Al、Al2O3、Fe和其它不溶于酸、碱的杂质)为原料生产NiSO4·7H2O晶体的两种工艺流程如下:
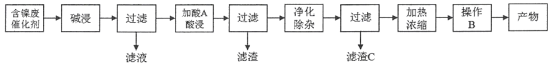
流程一:
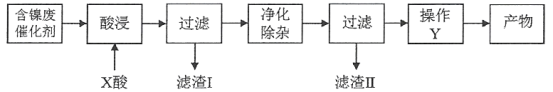
流程二:
已知:部分金属氢氧化物的Ksp近似值如下表所示:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
回答下列问题:
(1)流程一中所用酸A和流程二中所用酸X___________(填“相同”或“不相同”);流程一中滤渣C和流程二中滤渣II___________(填“相同”或“不相同”)。流程二中滤渣I是___________。
(2)流程一中“碱浸”时发生反应的离子方程式为_________________、___________________。
(3)流程二中“净化除杂”包含了两步操作过程:第一步,加入氧化剂H2O2,发生反应的离子方程式是____________________________________________;第二步,调节溶液的pH。
(4)分析比较流程一中操作B和流程二中操作Y后,回答操作Y是___________、___________、过滤、洗涤、干燥,即得产物。
(5)由己知信息列式计算:常温下,Ni2+完全沉淀时的pH值___________。
【答案】相同 不相同 其它不溶于酸、碱的杂质 2Al + 2OH- +2H2O=2AlO2- + 3H2↑ Al2O3 + 2OH- =2AlO2- + H2O 2Fe2++ H2O2+2H+= 2Fe3++2H2O 蒸发浓缩 冷却结晶 9
【解析】
流程一:由流程可知,某化工厂的含镍催化剂主要含有Ni,还含有Al、Al2O3、Fe和其它不溶于酸、碱的杂质,用NaOH碱浸时溶解Al和Al2O3,过滤得到固体是Ni、Fe和不溶于酸、碱的杂质,加入稀硫酸酸浸过滤,所得滤液主要含有Fe2+和Ni2+,加入过氧化氢氧化亚铁离子为铁离子,调节溶液pH使铁离子全部生成Fe(OH)3沉淀,镍离子不沉淀,过滤后调节溶液pH:2-3,以防止镍离子水解,通过蒸发浓缩,冷却结晶,过滤洗涤得到NiSO47H2O晶体;
流程二:某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其它不溶于酸、碱的杂质,工艺流程的目的是用含镍废催化剂制备NiSO47H2O晶体,分析工艺流程,将含Ni废催化剂用稀硫酸酸浸,则Ni、Al、Fe和Al2O3均溶于酸,得到Al3+、Fe2+和Ni2+,进行过滤操作,则不溶于酸的杂质被过滤出,滤液中主要含有Al3+、Fe2+和Ni2+,净化除杂主要除去Al3+、Fe2+,得到Ni2+的溶液,经过后续处理得到NiSO47H2O晶体,以此解答该题。
(1)由流程分析知:目标产物均为NiSO47H2O,则流程一中所用酸A和流程二中所用酸X均为稀硫酸;流程一中滤渣C为Fe(OH)3沉淀,而流程二中滤渣II为Al(OH)3和Fe(OH)3沉淀,则流程一中滤渣C和流程二中滤渣II不相同;流程二中滤渣I是其它不溶于酸、碱的杂质;
(2)流程一中“碱浸”时用NaOH溶液溶解Al和Al2O3,均生成NaAlO2,前者还有H2生成,发生反应的离子方程式为2Al + 2OH- +2H2O=2AlO2-+ 3H2↑、Al2O3 + 2OH-=2AlO2-+ H2O;
(3)流程二中“净化除杂”包含了两步操作过程:第一步,加入氧化剂H2O2,目的是氧化溶液中的Fe2+生成Fe3+,发生反应的离子方程式是2Fe2++ H2O2+2H+= 2Fe3++2H2O;
(4)流程二中从溶液中获得NiSO47H2O的操作Y是蒸发浓缩、冷却结晶、过滤、洗涤、干燥,即得产物。
(5)由Ksp(Ni(OH)2)=c(Ni2+)×c2(OH-)=10-15,Ni2+完全沉淀时c(Ni2+)<1×10-5mol/L,则Ni2+完全沉淀时的c(OH-)=![]() mol/L=1×10-5mol/L,此时溶液的pH=-lg
mol/L=1×10-5mol/L,此时溶液的pH=-lg![]() =9。
=9。