题目内容
11.下列物质都具有漂白作用,其中漂白原理没有利用物质化学性质的是( )| A. | 过氧化钠 | B. | 二氧化硫 | C. | 双氧水 | D. | 活性炭 |
分析 双氧水、Na2O2都是因为强氧化性而具有漂白作用,经它们漂白的物质,不能恢复原来的颜色,SO2的漂白是由于它跟某些有色物质化合生成了不稳定的无色物质,这些物质受热容易分解而恢复原来的颜色,中间发生了化合反应,活性炭具有吸附性而具有漂白作用.
解答 解:A.过氧化钠因为强氧化性而具有漂白作用,经它们漂白的物质,不能恢复原来的颜色,发生化学变化,故A错误;
B.SO2的漂白是由于它跟某些有色物质化合生成了不稳定的无色物质,这些物质受热容易分解而恢复原来的颜色,发生了化合反应,故B错误;
C.双氧水因为强氧化性而具有漂白作用,经它们漂白的物质,不能恢复原来的颜色,发生化学变化,故C错误;
D.活性炭具有吸附性而具有漂白作用,是物理变化过程,不涉及化学变化,故D正确.
故选D.
点评 本题考查了双氧水、活性炭、Na2O2、SO2几种物质的漂白性原理,注意相关知识的梳理和归纳是关键,难度不大.

练习册系列答案
相关题目
1.硫酸铵分解的化学方程式为 3(NH4)2SO4═4NH3↑+3X↑+N2↑+6H2O,则X的化学式为( )
| A. | S | B. | O2 | C. | SO2 | D. | SO3 |
2.分子式为CH2Cl2的有机物同分异构体共有(不考虑立体异构)( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
19.用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )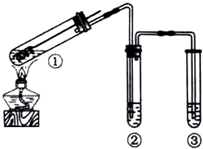

| A. | 为确认CuSO4生成,向①中加水,观察颜色 | |
| B. | 上下移动①中铜丝可控制SO2的量 | |
| C. | ②中选用品红溶液验证SO2的生成 | |
| D. | ③中选用NaOH溶液吸收多余的SO2 |
6.在1L0.1mol•L-1的NaHCO3溶液中,下列关系式正确( )
| A. | c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-) | B. | c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | ||
| C. | c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | D. | c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
16.下列各种有机物能发生加成、加聚、酯化、水解、中和反应的是( )
| A. | 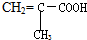 | B. | 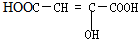 | C. | HCOOCH=CHCOOH | D. | CH2=C-COOCH3 |
3.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3.关于该物质的说法正确的是( )
| A. | 该物质属于两性氢氧化物 | |
| B. | 该药剂不适合于胃溃疡患者服用 | |
| C. | 1mol NaAl(OH)2CO3最多可消耗3molH+ | |
| D. | 该物质是Al(OH)3和Na2CO3的混合物 |
1.已知16S和52Te位于同一主族,下列关系正确的是( )
| A. | 原子半径:Te>Cl>S | B. | 热稳定性:H2Te>H2S>PH3 | ||
| C. | 还原性:Cl->S2->Te2- | D. | 酸性:HClO4>H2SO4>H2TeO4 |