题目内容
下列各组物质(用序号填空):
① 金刚石和石墨;
②1H、2H、3H;
③ CH4和C10H22;
④乙烷和(CH3)2CHCH2CH3;
⑤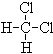 和
和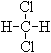 ;
;
⑥ CH3 (CH2) 3 CH3和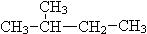
(1) 属于同一物质的是 ;
(2)互为同分异构体的是 ;
(3)互为同系物的是 ;
(4) 互为同素异形体的是 ;
(5) 互为同位素的是 。
(6分)(1)⑤. ;⑵ . ⑥;⑶ .③④ ;⑷. ① ;⑸. ②
解析试题分析:(1)性质和结构都完全相同的是同一种物质,所以属于同一种物质的是 和
和 ,答案选⑤。
,答案选⑤。
(2)分子式相同结构不同的化合物互为同分异构体,所以CH3 (CH2) 3 CH3和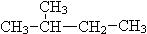 互为同分异构体,答案选⑥。
互为同分异构体,答案选⑥。
(3)结构相似,分子组成相差若干个CH2原子团的同一类有机物的,互称为同系物,则互为同系物的是CH4和C10H22和乙烷和(CH3)2CHCH2CH3,答案选③④。
(4)由同一种元素形成的不同单质互为同素异形体,所以互为同素异形体的是金刚石和石墨,答案选①。
(5)质子数相同,中子数不同的同一种元素的不同核素互称为同位素,所以互为同位素的是1H、2H、3H,答案选②。
考点:考查同系物、同分异构体、同位素、同素异形体以及同一种物质的判断
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。该题的关键是明确同系物、同分异构体、同位素、同素异形体以及同一种物质含义、判断依据,然后结合题意灵活运用即可。有利于培养学生的逻辑思维能力和发散思维能力。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案硫酸亚铁是一种重要的化工原料,可以制备一系列物质。下列说法错误的是( )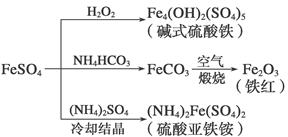
| A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
现有下列十种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:
| 分类标准 | | 氧化物 | | | 电解质 |
| 属于该类的物质 | ② | | ⑧⑨ | ⑦ | |
 H2O,该离子反应对应的化学方程式为 。
H2O,该离子反应对应的化学方程式为 。(3)⑩在水中的电离方程式为 ,17.1g⑩溶于水配成250mL溶液,SO42-的粒子数为 ,SO42-的物质的量浓度为 。
(4)少量的④通入⑥的溶液中反应的离子方程式为 。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),还原剂与氧化剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。
该反应的离子方程式为 。
FeCl3是一种用途比较广泛的盐。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。请写出反应的离子方程式 。
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是 (填字母序号)。
| A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可。 |
| B.在FeCl3溶液中加入足量的NaOH溶液 |
| C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体 |
| D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀 |
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+ 2KI = 2FeCl2+ I2+2KI,在上式上用双线桥法标出该反应电子转移的方向和数目。向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为 色,再将混合液倒入 (填仪器名称)中,将两层液体分离。
下列反应的离子方程式错误的是
| A.碘水加到溴化钠溶液中:2 Br-+ I2=== 2I- + Br2 |
| B.氯气通入碘化钾溶液中:2I-+ Cl2=== 2Cl-+ I2 |
| C.氯气溶于水:Cl2+ H2O === 2H+ + Cl-+ ClO- |
| D.硝酸银溶液中滴加碘化钠溶液:Ag+ + I- === AgI↓ |
(原创)下列离子方程式错误的是
| A.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| B.向KI溶液中加H2SO4溶液后振摇:4H+ + 4I-+ O2 = 2I2 + 2H2O |
| C.酸性高锰酸钾中加入草酸,溶液褪色:2MnO4- + 5H2C2O4 + 6 H+ = 2Mn2+ + 10CO2↑ +8H2O |
| D.证明C的非金属性强于Si的反应:SiO32-+ CO2+ H2O = H2SiO3↓+ CO32- |