题目内容
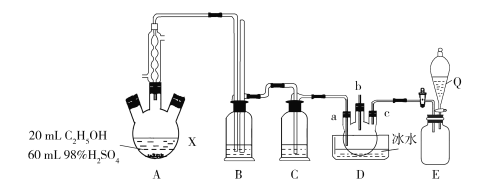
【题目】可用如图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
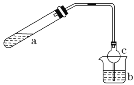
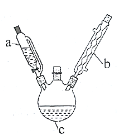
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是______。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是_____________________。
(3)实验中加热试管a的目的是:
①_____________________________________________________;
②______________________________________________________。
a中反应的化学方程式:__________________________________。
(4)球形干燥管c的作用是_________________________________, b烧杯中加有饱和Na2CO3溶液,其作用是_____________________。
(5)若反应前向b中加入几滴酚酞,溶液呈红色,反应结束后b中的现象是_____________。
【答案】先加入2 mL乙醇和2 mL冰醋酸混合物,然后一边摇动试管一边慢慢地加入2 mL浓硫酸 在试管中加入几片沸石(或碎瓷片) 加快反应速率 及时将产物乙酸乙酯蒸出,提高乙酸乙酯产率 CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 冷凝和防止倒吸 吸收蒸出的少量乙酸和乙醇,降低乙酸乙酯的溶解度 出现分层现象,下层红色变浅,上层是透明的油状液体
CH3COOCH2CH3+H2O 冷凝和防止倒吸 吸收蒸出的少量乙酸和乙醇,降低乙酸乙酯的溶解度 出现分层现象,下层红色变浅,上层是透明的油状液体
【解析】
(1)根据浓硫酸稀释的原理,确定添加顺序;
(2)液体加热要加碎瓷片,防止暴沸;
(3)实验中加热试管的目的是提供能量;
(4)从产物的收集、分离与提纯角度分析;
(5)根据碳酸钠与乙酸的反应以及乙酸乙酯的密度进行解答。
(1)为防止酸液飞溅,先加入2 mL乙醇和2 mL冰醋酸混合物,然后一边摇动试管一边慢慢地加入2 mL浓硫酸;故答案为:先加入2 mL乙醇和2 mL冰醋酸混合物,然后一边摇动试管一边慢慢地加入2 mL浓硫酸;
(2)为了防止发生暴沸应在加热前向试管中加入几片沸石(或碎瓷片);故答案为:在试管中加入几片沸石(或碎瓷片);
(3)加热试管可提高反应效率,同时可将乙酸乙酯及时蒸出,有利于提高乙酸乙酯的产率;a中反应的化学方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;故答案为:加快反应速率;及时将产物乙酸乙酯蒸出,提高乙酸乙酯产率;CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;故答案为:加快反应速率;及时将产物乙酸乙酯蒸出,提高乙酸乙酯产率;CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(4)由于乙醇与乙酸都易挥发,制备的乙酸乙酯中含有乙醇与乙酸,通常用饱和碳酸钠溶液收集乙酸乙酯,中和挥发出来的乙酸,使之转化为易溶于水的乙酸钠,溶解挥发出来的乙醇,并降低乙酸乙酯在水中的溶解度,便于分层得到酯,由于乙醇与乙酸均易溶于水,因此用Na2CO3溶液吸收产物时应意防止倒吸;故答案为:冷凝和防止倒吸;吸收蒸出的少量乙酸和乙醇,降低乙酸乙酯的溶解度;
(5)开始反应前b中存在Na2CO3,所以滴入酚酞溶液呈红色,而反应结束后产物中除乙酸乙酯外,还有伴随蒸出的乙醇和乙酸,少量的乙酸中和掉b中的OH-,从而使红色变浅,并且生成的乙酸乙酯不溶于水,密度比水小,所以出现分层现象;故答案为:出现分层现象,下层红色变浅,上层是透明的油状液体。

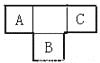
【题目】4种相邻的主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。回答下列问题:
m | n | ||
x | y |
(1)元素x在周期表中的位置是第_____周期、第____族,其单质可采用电解熔融的_____方法制备。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是______,碱性最强的是______.(填化学式)
(3)气体分子(mn)2的电子式为_______,(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是_____________________________。