题目内容
【题目】1,2二氯乙烷是一种广泛使用的有机溶剂、黏合剂,也用作谷物和粮仓的熏蒸剂,沸点83.5 ℃,熔点35 ℃。某研究性学习小组的同学利用下图(加热装置省略)装置制备一定量的 1,2二氯乙烷,制备原理为:C2H5OH![]() C2H4
C2H4![]() CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8 g·mL1。
CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8 g·mL1。
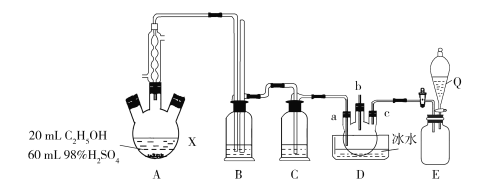
(1)根据制备原理,可知装置A中还缺少的一种实验仪器是_____。使用冷凝管的目的是_______。
(2)实验时A中三颈烧瓶内有刺激性气味的无机气体产生,为吸收反应中生成的无机气体,在装置B中应加入________(填字母)。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)D中a、c两个导管进入仪器中的长度不同,其优点是________,对导管b的进一步处理方法是_____________,装置E是氯气的贮气瓶,则Q中的物质是______________。
(4)写出D中反应的化学方程式________________________。
(5)若得到a g 1,2-二氯乙烷,则乙醇的利用率为___________。
【答案】温度计 使乙醇冷凝回流,提高原料的利用率 c 有利于Cl2、C2H4充分混合反应 将用b管逸出的Cl2引入到NaOH溶液中 饱和食盐水 CH2=CH2+ Cl2![]() CH2ClCH2Cl
CH2ClCH2Cl ![]()
【解析】
(1)A中反应需控制温度在170 ℃,所以还缺少的仪器是温度计。由于反应温度高于乙醇的沸点,反应中会有大量的乙醇气化,因此使用冷凝管的目的是使已经气化的乙醇冷凝回流,提高乙醇的利用率。
(2)浓硫酸能使乙醇碳化生成单质碳,C与浓硫酸反应生成的CO2、SO2,可用NaOH溶液吸收除去。
(3)C2H4密度小而Cl2的密度大,按图中方式将两种气体通入到容器中,有利于二者充分混合反应。Cl2有毒且在容器中难以完全反应,故要将从b中逸出的Cl2通入到NaOH溶液中,防止其污染空气。Q中液体下滴,从而将Cl2排入到D中,因此Cl2不能被Q中液体吸收或溶解,故Q中是饱和食盐水。
(5)由C2H5OH~C2H4Cl2可求出转化为C2H4Cl2的乙醇质量为46a/99 g,20 mL乙醇质量为16 g,故乙醇的利用率为![]() 。
。
(1)A中反应需控制温度在170 ℃,所以还缺少的仪器是温度计。由于反应温度高于乙醇的沸点,反应中会有大量的乙醇气化,因此使用冷凝管的目的是使已经气化的乙醇冷凝回流,提高乙醇的利用率,答案为:温度计;使乙醇冷凝回流,提高原料的利用率。
(2)浓硫酸能使乙醇碳化生成单质碳,C与浓硫酸反应生成的CO2、SO2,可用NaOH溶液吸收除去,答案为:c。
(3)C2H4密度小而Cl2的密度大,按图中方式将两种气体通入到容器中,有利于二者充分混合反应。Cl2有毒且在容器中难以完全反应,故要将从b中逸出的Cl2通入到NaOH溶液中,防止其污染空气。Q中液体下滴,从而将Cl2排入到D中,因此Cl2不能被Q中液体吸收或溶解,故Q中是饱和食盐水,答案为:有利于Cl2、C2H4充分混合反应;将用b管逸出的Cl2引入到NaOH溶液中;饱和食盐水。
(4)装置D中为乙烯与氯气的加成反应,其反应式为:CH2=CH2+ Cl2![]() CH2ClCH2Cl;
CH2ClCH2Cl;
(5)由C2H5OH~C2H4Cl2可求出转化为C2H4Cl2的乙醇质量为46a/99 g,20 mL乙醇质量为16 g,故乙醇的利用率为![]() 。
。

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案