��Ŀ����
����Ŀ����ͼΪһ��������ˮ����װ�ã���װ�ÿ�����һ�����ォ�л���ˮ�Ļ�ѧ��ֱ��ת��Ϊ���ܣ���ͼ��һ���ö��Ե缫��ⱥ��ʳ��ˮ������Һ�����������ڼס��ҵ�˵����ȷ����

A. װ�����е�b��Ҫ��װ�ü�X������
B. װ������a���ĵ缫��ӦʽΪ:2Cl- -2e-=Cl2��
C. ��N������5.6L(��״����)����ʱ������2NA��H+ͨ�����ӽ���Ĥ
D. ���л���ˮ����Ҫ���������ǣ���װ�ü���M�������ĵ缫��ӦΪ: C6H12O6+6H2O-24e-=6CO2��+24H+
���𰸡�D
������������֪���ͼʾ����Ϊԭ��أ�XΪ������YΪ��������Ϊ�ö��Ե缫��ⱥ��ʳ��ˮ������Һ����������aΪ��������������NaOH��bΪ��������Cl2��������Cl2��NaOH��Ӧ����NaClO��
A�bΪ����������Ӧ��������(Y��)���ӣ���A����B�aΪ�������缫��ӦʽΪ��2H2O+2e-=2OH-+H2����bΪ�������缫��ӦʽΪ��2Cl--2e-=Cl2������B����C���ͼ��N�缫Ϊ�����õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ��O2+4H++4e-=2H2O����N�缫����5.6L(��״����)����(��0.25mol)ʱ������1mol�����ӣ�����NA��H+ͨ�����ӽ���Ĥ����C����D����л���ˮ����Ҫ���������ǣ���װ�ü���M������C6H12O6ʧ���ӵ�������Ӧ�����ɶ�����̼�����ݵ���غ��ԭ���غ㣬��缫ӦΪ��C6H12O6+6H2O-24e-=6CO2��+24H+����D��ȷ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ʮ�������������ϵ����ʲ��ϱ仯�������ijɷ�Ҳ�����˺ܴ�ı仯���±���Ŀǰ������ԭʼ��������Ҫ�ɷ֣�
Ŀǰ��������Ҫ�ɷ� |
|
ԭʼ��������Ҫ�ɷ� |
|
���ϱ����漰�ķ�����д���пհף�
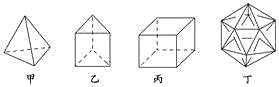
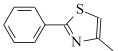
��1������10�����ӵķ�����__________���ѧʽ����ͬ����
��2���ɼ��Լ����ɵķǼ��Է�����________��
��3����![]() ��ֱ���γ���λ���ķ�����________
��ֱ���γ���λ���ķ�����________
��4�������µ��ӶԵķ��ӣ�ϡ��������⣩��______���������幹��Ϊ_______��
��5����������ˮ��ˮ��Һ�ʼ��Եķ�����__________����֮���Լ�������ˮ����Ϊ���ķ��Ӻ�ˮ����֮���γ���______��
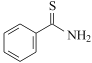
��6��![]() �Ľṹ�ɱ�ʾΪ
�Ľṹ�ɱ�ʾΪ![]() ����
����![]() �ṹ�����Ƶķ�����______�������ֽṹ���Ƶķ��ӵļ���__________��������ͬ����������ͬ������
�ṹ�����Ƶķ�����______�������ֽṹ���Ƶķ��ӵļ���__________��������ͬ����������ͬ������![]() ��������һ�������γ���������������ͬ������_______��
��������һ�������γ���������������ͬ������_______��
����Ŀ��ijѧ����0.2000molL-1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����
��������ˮϴ�Ӽ�ʽ�ζ��ܣ���ע��NaOH��Һ����0���̶�������
�ڹ̶��õζ��ܲ�ʹ�ζ��ܼ������Һ��
�۵���Һ������0����0���̶������£������¶���
����ȡ20.00mL����Һע��ྻ����ƿ�У�������3mL��̪��Һ
���ñ�Һ�ζ����յ㣬���µζ���Һ�������ش�
��1�����ϲ����д������___(����)��
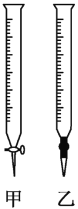
��2���ñ�NaOH��Һ�ζ�ʱ��Ӧ����NaOH��Һע��___(��ͼ��ѡ����������������)�С�
��3�����в���������ʵ����ƫ�����___(����)��
A.����ƿװҺǰ��������������ˮ
B.�ζ�ǰ���ζ��ܼ��������ݣ��ζ���������
C.����ʽ�ζ�����ȡҺ��ʱ���ͷ�Һ��ǰ�ζ���ǰ�������ݣ�֮����ʧ
��4���ζ�ʱ�����ֿ��Ƶζ��ܣ�����ҡ����ƿ���۾�ע��___���жϵ���ζ��յ�������ǣ���ƿ����Һ___��
��5��������ʵ�����ݼ�¼����
�ζ����� | �������(mL) | NaOH��Һ�������(mL) | |
�ζ�ǰ | �ζ��� | ||
1 | 20.00 | 0.00 | 21.30 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.32 |
ͨ������ɵã�������Ũ��Ϊ___ molL-1(����������4λС��)��