题目内容
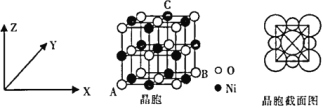
【题目】过渡元素在生活、生产和科技等方面有广泛的用途。
(1)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是________(填序号)。
A.PFS中铁显+2价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
Mn | Fe | ||
电离能 | I1 | 717 | 759 |
(kJ·mol-1) | I2 | 1 509 | 1 561 |
I3 | 3 248 | 2 957 |
(2)PFS中SO42-采取__________杂化,空间构型是_________。
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬与甲基丙烯酸根的配合物为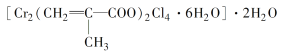
①该化合物中铬的化合价为___________。
②该化合物中一个Cr的配位数为________。
③甲基丙烯酸分子中C原子的杂化方式有___________________________________。
(4)O、S、Se为同主族元素,H2O、H2S和H2Se的参数对比见表.
化学式 | 键长/nm | 键角 |
H2O | 0.99 | 104.5° |
H2S | 1.34 | 92.3° |
H2Se | 1.47 | 91.0° |
H2S的键角大于H2Se的原因可能为__________________________________________________
【答案】ADsp3正四面体+36sp3和sp 2由于硫的电负性强于Se,形成的共用电子对斥力大,键角大
【解析】
(1)A.设[Fe2(OH)n(SO4)3-n/2]m中Fe元素化合价为x,根据化合价代数和为0,可知2x-n+(3-![]() )×(-2)=0,解得x=+3,选项A不正确;B.Fe原子核外电子数为26,铁元素的价电子数8,且4s轨道排2个电子,3d轨道排6个电子,所以铁原子的价电子排布式是3d64s2,选项B正确;C.硫酸亚铁中铁元素的化合价是+2价,[Fe2(OH)n(SO4)3-n/2]m中铁元素的化合价是+3价,铁离子水解生成氢氧化铁,所以由FeSO4溶液制PFS需经过氧化、水解和聚合的过程,选项C正确;D.Fe2+再失去一个电子需要的能量比气态Mn2+再失去一个电子需要能量小,所以气态Fe2+再失去一个电子比气态Mn2+再失去一个电子容易,选项D不正确;答案选AD;
)×(-2)=0,解得x=+3,选项A不正确;B.Fe原子核外电子数为26,铁元素的价电子数8,且4s轨道排2个电子,3d轨道排6个电子,所以铁原子的价电子排布式是3d64s2,选项B正确;C.硫酸亚铁中铁元素的化合价是+2价,[Fe2(OH)n(SO4)3-n/2]m中铁元素的化合价是+3价,铁离子水解生成氢氧化铁,所以由FeSO4溶液制PFS需经过氧化、水解和聚合的过程,选项C正确;D.Fe2+再失去一个电子需要的能量比气态Mn2+再失去一个电子需要能量小,所以气态Fe2+再失去一个电子比气态Mn2+再失去一个电子容易,选项D不正确;答案选AD;
(2)PFS中SO42-总价电子数32,中心原子有4个σ键,采取sp3杂化,空间构型是正四面体立体结构;
(3)①该化合物中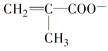 显-1价,氯元素为-1价,则铬的化合价为+3价;②2个Cr共有12个配体,则一个Cr的配位数为6;③甲基上的碳原子含有4个σ键,所采取sp3杂化,碳碳双键上的碳原子含有3σ键,所以采取sp2杂化;
显-1价,氯元素为-1价,则铬的化合价为+3价;②2个Cr共有12个配体,则一个Cr的配位数为6;③甲基上的碳原子含有4个σ键,所采取sp3杂化,碳碳双键上的碳原子含有3σ键,所以采取sp2杂化;
(4)根据表中数据可知,由于硫的电负性强于Se,形成的共用电子对斥力大,键角大。

 阅读快车系列答案
阅读快车系列答案