题目内容
【题目】材料的不断发展可以促进社会的进步,性能各异的各种材料的广泛应用大大提高了人们的生活水平。回答下列问题:
(1)橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为体型结构,从而增大橡胶的强度,橡胶属于____(填字母)。
a. 无机非金属材料 b. 金属材料 c. 有机高分子材料
保持洁净安全的生存环境已成为全人类的共识。
(2)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行__________________ 。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为 ___________________________________________ 。
(3)获得洁净安全的饮用水是每个人的正常需要。某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为______________________________ 。
(4)天然水中含有细小悬浮颗粒或胶体颗粒,可以用 ____ (填一种物质的化学式)作为混凝剂净化处理。明矾净水工作原理的离子方程式为_____________。
【答案】C脱硫处理2NO+2CO![]() N2+2CO2Ca(ClO)2+H2O+CO2=CaCO3+2HClOKAl(SO4)2·12H2OAl3++ 3H2O
N2+2CO2Ca(ClO)2+H2O+CO2=CaCO3+2HClOKAl(SO4)2·12H2OAl3++ 3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
【解析】
(1)天然橡胶是天然有机高分子化合物,天然橡胶通过硫化处理,使它的分子转化为体型结构,从而增大橡胶的强度,橡胶属于有机高分子材料;
(2)大气中的SO2主要是化石燃料燃烧造成的, 为了控制SO2的排放, 常采取的措施是对化石燃料进行脱硫处理, 汽车尾气中主要是CO、NO、NO2和碳氢化合物, 其中NO、CO在催化剂的作用下生成无毒物质N2和CO2,方程式为:2NO+2CO![]() N2+2CO2;
N2+2CO2;
(3)用漂白粉和漂白精片进行杀菌消毒, 主要是利用空气中的CO2与Ca(ClO)2反应生成HClO的强氧化性, 反应方程式为: Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
(4)明矾可用于净水,因为溶于水铝离子水解生成氢氧化铁胶体,胶体具有吸附性,可用于净水,明矾的化学式为KAl(SO4)2·12H2O,净水工作原理的离子方程式为Al3++ 3H2O![]() Al(OH)3(胶体)+3H+。
Al(OH)3(胶体)+3H+。

【题目】过渡元素在生活、生产和科技等方面有广泛的用途。
(1)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是________(填序号)。
A.PFS中铁显+2价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
Mn | Fe | ||
电离能 | I1 | 717 | 759 |
(kJ·mol-1) | I2 | 1 509 | 1 561 |
I3 | 3 248 | 2 957 |
(2)PFS中SO42-采取__________杂化,空间构型是_________。
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬与甲基丙烯酸根的配合物为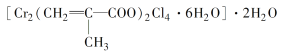
①该化合物中铬的化合价为___________。
②该化合物中一个Cr的配位数为________。
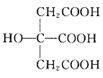
③甲基丙烯酸分子中C原子的杂化方式有___________________________________。
(4)O、S、Se为同主族元素,H2O、H2S和H2Se的参数对比见表.
化学式 | 键长/nm | 键角 |
H2O | 0.99 | 104.5° |
H2S | 1.34 | 92.3° |
H2Se | 1.47 | 91.0° |
H2S的键角大于H2Se的原因可能为__________________________________________________