题目内容
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)制备精细化工产品PbSO4·3PbO·H2O(三盐)的主要流程如下:

已知:常温下,Ksp(PbSO4)=2.0×10-8 Ksp(PbCO3)=1.0×10-13 ,请回答以下问题:
(1)铅蓄电池工作原理是PbO2+Pb+2H2SO4![]() 2PbSO4+2H2O,在放电过程中负极的质量__________;电解质溶液的pH___________(用“变大”、“不变”或“变小”填写)。该铅蓄电池放电过程中的正极反应式为__________________________________________。
2PbSO4+2H2O,在放电过程中负极的质量__________;电解质溶液的pH___________(用“变大”、“不变”或“变小”填写)。该铅蓄电池放电过程中的正极反应式为__________________________________________。
(2)步骤③的目的是使铅泥中的Pb溶解,其对应的离子方程式为________________ 。滤液2中的溶质主要是_____________(填化学式),过滤操作中使用到的玻璃仪器有_____。
(3)步骤⑥合成三盐的化学方程式为________________________。
(4)步骤⑦洗涤产品的方法是________________________________。
(5)在“转化”过程中,若PbSO4和PbCO3在悬浊液中共存,则c(SO42-):c(CO32-)=____________。
【答案】变大 变大 PbO2+SO42-+4H++2e-=PbSO4+2H2O 3Pb+8H++2NO3-=3Pb2++2NO+4H2O HNO3 玻璃棒、烧杯、漏斗 4PbSO4+6NaOH=3Na2SO4+PbSO43PbOH2O+2H2O 将产品放入过滤器中,加入蒸馏水没过产品,让谁自然流下,重复2至3次 2.0×105
【解析】
题时抓住流程中物质转化原理及铅蓄电池工作原理,分析元素化合价变化,弄清滤液和滤渣的主要成分,根据物质性质推断相关的化学反应;区别放电和充电,根据电极反应类型书写电极反应式。
(1)铅蓄电池工作原理是PbO2+Pb+2H2SO4![]() 2PbSO4+2H2O,在放电过程中负极电极反应式:Pb+ H2SO4-2e-=PbSO42-+4H+,所以负极的质量变大;放电时,正极的电极反应式为PbO2+2e-+ SO42-+4H+
2PbSO4+2H2O,在放电过程中负极电极反应式:Pb+ H2SO4-2e-=PbSO42-+4H+,所以负极的质量变大;放电时,正极的电极反应式为PbO2+2e-+ SO42-+4H+![]() PbSO4+2H2O,电解质溶液的H+浓度减小,所以pH变大。答案:变大;变大 ; PbO2+SO42-+4H++2e-=PbSO4+2H2O。
PbSO4+2H2O,电解质溶液的H+浓度减小,所以pH变大。答案:变大;变大 ; PbO2+SO42-+4H++2e-=PbSO4+2H2O。
(2)步骤③的目的是使铅泥中的Pb溶解,其对应的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO+4H2O 。沉铅涉及的反应为Pb(NO3)2+H2SO4![]() PbSO4↓+2HNO3。所以滤液Ⅱ中的溶质主要是HNO3,过滤操作中使用到的玻璃仪器有玻璃棒、烧杯、漏斗。答案: 3Pb+8H++2NO3-=3Pb2++2NO+4H2O ; HNO3 ;玻璃棒、烧杯、漏斗。
PbSO4↓+2HNO3。所以滤液Ⅱ中的溶质主要是HNO3,过滤操作中使用到的玻璃仪器有玻璃棒、烧杯、漏斗。答案: 3Pb+8H++2NO3-=3Pb2++2NO+4H2O ; HNO3 ;玻璃棒、烧杯、漏斗。
(3) 加入NaOH溶液,合成三盐的化学方程式为4PbSO4+6NaOH![]() 3PbO·PbSO4·H2O↓+3Na2SO4+2H2O。答案:4PbSO4+6NaOH=3Na2SO4+PbSO43PbOH2O+2H2O
3PbO·PbSO4·H2O↓+3Na2SO4+2H2O。答案:4PbSO4+6NaOH=3Na2SO4+PbSO43PbOH2O+2H2O
(4) 向装产品的过滤器中加入蒸馏水没过产品,让水自然流下,重复2至3次即可;答案:将产品放入过滤器中,加入蒸馏水没过产品,让水自然流下,重复2至3次 。
(5) PbSO4(s)+ CO32-(aq)![]() PbCO3(s)+ SO42-(aq);K=c(SO42-)/c(CO32-)= Ksp(PbSO4)/ Ksp(PbCO3)=2.0×10-8/1.0×10-13 ==2.0×105。所以在转化过程中,PbSO4和PbCO3在悬浊液中共存时,则c(SO42-):c(CO32-)=2.0×105。答案:2.0×105。
PbCO3(s)+ SO42-(aq);K=c(SO42-)/c(CO32-)= Ksp(PbSO4)/ Ksp(PbCO3)=2.0×10-8/1.0×10-13 ==2.0×105。所以在转化过程中,PbSO4和PbCO3在悬浊液中共存时,则c(SO42-):c(CO32-)=2.0×105。答案:2.0×105。

【题目】过渡元素在生活、生产和科技等方面有广泛的用途。
(1)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是________(填序号)。
A.PFS中铁显+2价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
Mn | Fe | ||
电离能 | I1 | 717 | 759 |
(kJ·mol-1) | I2 | 1 509 | 1 561 |
I3 | 3 248 | 2 957 |
(2)PFS中SO42-采取__________杂化,空间构型是_________。
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬与甲基丙烯酸根的配合物为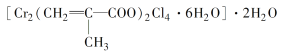
①该化合物中铬的化合价为___________。
②该化合物中一个Cr的配位数为________。
③甲基丙烯酸分子中C原子的杂化方式有___________________________________。
(4)O、S、Se为同主族元素,H2O、H2S和H2Se的参数对比见表.
化学式 | 键长/nm | 键角 |
H2O | 0.99 | 104.5° |
H2S | 1.34 | 92.3° |
H2Se | 1.47 | 91.0° |
H2S的键角大于H2Se的原因可能为__________________________________________________