题目内容
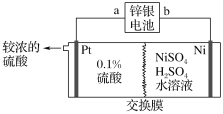
【题目】锌银电池的负极为锌,正极为氧化银,电解质是KOH,电池反应为Zn+Ag2O+H2O=Zn(OH)2+2Ag。以锌银电池为电源,电解硫酸镍溶液冶炼纯镍,装置如图所示。下列说法正确的是( )
A.装置中使用阳离子交换膜
B.锌银电池a极反应式为Ag2O+H2O+2e-=2Ag+2OH-
C.左侧若加入稀盐酸,电解后得到比较浓的盐酸
D.若锌银电池溶解13 g锌,则镍极净增质量最多为5.9 g
【答案】B
【解析】
A. 根据左侧是稀硫酸进,较浓的硫酸流出,装置中使用阴离子交换膜,故A错误;
B. b是负极,a是正极,得电子,发生还原反应,锌银电池a极反应式为Ag2O+H2O+2e-=2Ag+2OH-,故B正确;
C. 左侧若加入稀盐酸,Cl-的还原性比OH-强,电解后得不到比较浓的盐酸,故C错误;
D. 由电子守恒得关系式:Zn~2e-~Ni,若锌银电池溶解13 g锌,则镍极净增质量最多为![]() =11.8 g,故D错误;
=11.8 g,故D错误;
故选B。

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目