题目内容
【题目】分别调节0.01mol·L-1HCOOH溶液、0.01mol·L-1氨水的pH,系统中微粒浓度的负对数值(-lgc)与pH的关系分别如下图所
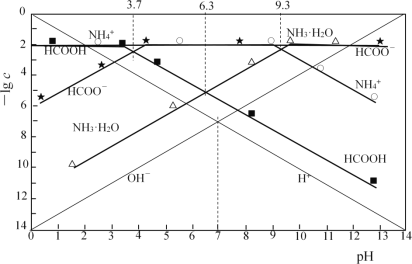
下列说法错误的是
A. 25℃时,NH3·H2O![]() NH4++OH-的lgK=-4.7
NH4++OH-的lgK=-4.7
B. 25℃时,0.01mol·L-1HCOOH溶液的pH为3.7
C. HCOONa溶液中加入NH4Cl至溶液呈中性:c(Cl-)>c(Na+)>c(HCOO-)
D. HCOONa溶液中加入KHSO3至溶液呈中性:c(HCOOH) +c(H2SO3) = c(SO32-)
【答案】BC
【解析】
-
A、NH3·H2O为弱碱,部分电离,电离平衡常数只受温度的影响,因此25℃时当c(NH3·H2O)=c(NH4+),K=c(OH-)=Kw/c(H+)=10-4.7mol·L-1,即lgK=-4.7,故A说法正确;
B、25℃时甲酸的平衡常数为K=10-3.7,根据平衡常数,25℃时,0.01mol·L-1甲酸中c(H+)=10-2.85mol·L-1,即pH≈2.9,故B错误;
C、根据水解平衡常数、电离平衡常数、水的离子积之间的关系,HCOO-的水解平衡常数Kh=Kw/Ka=10-10.3,NH4+的水解平衡常数Kh=10-9.3,NH4+的水解程度大于HCOO-水解程度,两种溶液混合后呈中性,甲酸钠的量比NH4Cl多,Na+浓度大于Cl-浓度,故C错误;
D、根据电荷守恒,c(CHOO-)+c(HSO3-)+2c(SO32-)+c(OH-)=c(Na+)+c(H+)+c(K+),溶液显中性,c(H+)=c(OH-),即c(CHOO-)+c(HSO3-)+2c(SO32-)=c(Na+)+c(K+),根据物料守恒,c(Na+)=c(HCOO-)+c(HCOOH),c(K+)=c(HSO3-)+c(H2SO3)+c(SO32-),三式合并得到:c(SO32-)=c(HCOOH)+c(H2SO3),故D正确;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案