题目内容
【题目】煤矸石(主要成份是SiO2和Al2O3还含有少量的Fe2O3、K2O、TiO2)活化后,可以制备六水三氯化铝(AlCl3·6H2O),工艺流程如下图所示。

回答下列问题:
(1)焙烧至700℃左右可使煤矸石活化,活化过程中会发生一系列反应,写出SiO2与K2O反应的化学方程式______________,焙烧后的矸石颗粒有微孔,不需研磨成粉即可进行酸溶,原因是_____________。
(2)本工艺的突出特点是通过向饱和溶液中通HCl来得到产品和对一次残渣进行二次酸浸,HCl的作用是_________________和抑制Al3+水解,二次酸浸的目的是___________________。
(3)四轮循环后所得结晶滤液中,含有较多杂质离子,必须在常温下进行如下图所示的处理

已知:Ksp(Fe(OH)3]=1.0×10-38,Ksp(Al(OH)3]=1.0×10-33,当离子浓度等于1.0×10-5mol·L-1时,可认为其已沉淀完全。
滤渣1中所含金属元素为___________,获得滤渣2时,应调节溶液的pH至少为_________,在该流程中,滤渣3可循环使用,则生成滤渣2的离子方程式为_________________。
【答案】SiO2+K2O![]() K2SiO3 矸石颗粒有微孔,与酸溶液接触面积较大 降低产品的溶解度 提高原料的利用率 Ti(或钛) 3 Fe3++ Al(OH)3 =Fe(OH)3+Al3+
K2SiO3 矸石颗粒有微孔,与酸溶液接触面积较大 降低产品的溶解度 提高原料的利用率 Ti(或钛) 3 Fe3++ Al(OH)3 =Fe(OH)3+Al3+
【解析】
(1)SiO2是酸性氧化物与碱性氧化物反应生成含氧酸盐,SiO2与K2O反应的化学方程式:SiO2+K2O![]() K2SiO3 ;焙烧后的矸石颗粒有微孔,不需研磨成粉即可进行酸溶,矸石颗粒有微孔,与酸溶液接触面积较大;(2)本工艺的突出特点是通过向饱和溶液中通HCl,来得到产品和对一次残渣进行二次酸浸,HCl的作用是降低产品的溶解度和抑制Al3+水解,二次酸浸的目的是:提高原料的利用率;(3)当离子浓度等于1.0×10-5mol·L-1时,由Ksp(Fe(OH)3]=1.0×10-38,c(OH-)=
K2SiO3 ;焙烧后的矸石颗粒有微孔,不需研磨成粉即可进行酸溶,矸石颗粒有微孔,与酸溶液接触面积较大;(2)本工艺的突出特点是通过向饱和溶液中通HCl,来得到产品和对一次残渣进行二次酸浸,HCl的作用是降低产品的溶解度和抑制Al3+水解,二次酸浸的目的是:提高原料的利用率;(3)当离子浓度等于1.0×10-5mol·L-1时,由Ksp(Fe(OH)3]=1.0×10-38,c(OH-)=![]() =1.0×10-11mol·L-1,pH=3时铁沉淀完全;同理,Ksp(Al(OH)3]=1.0×10-33,c(OH-)=
=1.0×10-11mol·L-1,pH=3时铁沉淀完全;同理,Ksp(Al(OH)3]=1.0×10-33,c(OH-)=![]() =4.6×10-10mol·L-1,pH=4.6时铝沉淀完全;滤渣1中所含金属元素为Ti(或钛),滤渣2的主要成分是氢氧化铁,pH=3时铁沉淀完全,获得滤渣2时,应调节溶液的pH至少为3,在该流程中,滤渣3主要成分是氢氧化铝,可循环使用,则生成滤渣2的离子方程式为 Fe3++ Al(OH)3 =Fe(OH)3+Al3+。
=4.6×10-10mol·L-1,pH=4.6时铝沉淀完全;滤渣1中所含金属元素为Ti(或钛),滤渣2的主要成分是氢氧化铁,pH=3时铁沉淀完全,获得滤渣2时,应调节溶液的pH至少为3,在该流程中,滤渣3主要成分是氢氧化铝,可循环使用,则生成滤渣2的离子方程式为 Fe3++ Al(OH)3 =Fe(OH)3+Al3+。

【题目】用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)

A. 用装置甲检验溶液中是否有K+
B. 用装置乙制取并收集少量NH3
C. 用装置丙进行喷泉实验
D. 用装置丁加热熔融NaOH固体
【题目】某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如下:
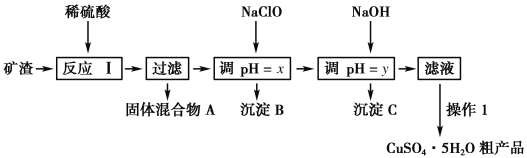
已知:①Cu2O+2H+===Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)为了加快反应Ⅰ的速率,可以采取的措施是____________ (写两条)。
(2)固体混合物A中的成分是________。
(3)反应Ⅰ完成后,铁元素的存在形式为________(填离子符号);写出生成该离子的离子方程式____________。
(4)操作1主要包括:蒸发浓缩、冷却结晶、________。洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是______________。
(5)用NaCl0调pH可以生成沉淀B,利用题中所给信息分析沉淀B为_______,该反应的离子方程式为______________.