��Ŀ����
����Ŀ������ѧ�Cѡ��3�����ʽṹ�����ʣ�̼����������þ����������ͭ�Ǽ�����Ҫ��Ԫ�أ���ش��������⣺
(1)�ڵڶ����ڵ�Ԫ���У���һ�����ܽ���B��N֮���Ԫ����_________�֡�
(2)����������Ϸ���MgO���۵��CuO���۵�ߵö࣬��ԭ����_____________��
(3)Fe��CO���γ�һ����Ҫ�Ĵ���Fe(CO)5���÷���������������������Ϊ______________����д��һ����CO��Ϊ�ȵ���������ӣ�________________��

(4)��������һ������ɫ����Ӳ����ʴ�Ľ��������Ļ���������࣬�磺Gr2(SO4)3��K2Cr2O7�Լ�������[Cr(H2O)3(NH3)3]3+��
��K2Cr2O7���к�ǿ�������ԣ���ֱ�ӽ�CH3CH2OH������CH3COOH����д����̬��ԭ�ӵļ۲�����Ų�ʽ__________��CH3COOH������̼ԭ�ӵ��ӻ�����Ϊ___________��
�ڸ�������[Cr(H2O)3(NH3)3]3+�У��������ӵ���λ��Ϊ_______��NH3��VSEPRģ��Ϊ_______��
��ͭ���Ͻ�ľ�����ͼ��ʾ����֪������Cr��Cuԭ�Ӽ���������Ϊ![]() apm,��þ�����ܶ�Ϊ_______g��cm-3(�ú�a�Ĵ���ʽ��ʾ����NAΪ�����ӵ�������ֵ)��
apm,��þ�����ܶ�Ϊ_______g��cm-3(�ú�a�Ĵ���ʽ��ʾ����NAΪ�����ӵ�������ֵ)��
���𰸡�3 Mg2+�뾶��Cu2+�뾶С��MgO�ľ����ܱ�CuO�ߣ����MgO���۵�� 1��1 C22-��CN- d54s1 sp3��sp2 6 �������� ![]()
��������
ͬ���ڣ��������ҵ�һ������������ȫ�����Ͱ����ԭ���֢�A��͢�A�塢��A��͢�A���һ�����ܷ�����Mg2+�뾶��Cu2+�뾶С��MgO�ľ����ܱ�CuO�ߣ�Fe��CO��5�к���6���Ҽ���2���м����ȵ�������ԭ�����ͼ۵���������ͬ��Cr��ԭ������Ϊ24����4�����Ӳ㣬����������Ϊ1������ΪCH3COOH������C�γ�4�����۵�����-COOH��C�γ�1��˫����2��������������[Cr(H2O)3(NH3)3]3+�У�Cr3=Ϊ��λ�壬H2O��NH3Ϊ��λ�壻���������м۲���ӶԸ���Ϊ4��
��1��ͬ���ڣ��������ҵ�һ������������ȫ�����Ͱ����ԭ���֢�A��͢�A�塢��A��͢�A���һ�����ܷ�����ڶ�����Ԫ���У���һ�����ܽ���B��N֮���Ԫ����Be��C��O����3�֡���2�����ӵ���������Ӱ뾶С�ľ����ܴ���Ӧ����Ϊ�۵�ߡ�Ӳ�ȴ�Mg2+��Cu2+���������ͬ������ǰ�߰뾶�Ⱥ���С����Ӧ����Ϊ�����ܴ��۵��3��Fe��CO��5�к���6���Ҽ���2���м����ʦҼ���м�����Ŀ֮��Ϊ3��1��C22����CN-��CO��ԭ��������2���۵���������10����Ϊ�ȵ����塣��4��Cr��ԭ������Ϊ24����4�����Ӳ㣬����������Ϊ1����̬��������Ų�ʽΪ1s22s22p63s23p6
3d54s1����۲�����Ų�ʽ 3d54s1������ΪCH3COOH������C�γ�4�����۵�����-COOH��C�γ�1��˫����2����������C���ӻ���ʽ�ֱ�Ϊsp3��sp2��������[Cr(H2O)3(NH3)3]3+�У�Cr3=Ϊ��λ�壬H2O��NH3Ϊ��λ�壬������λ��Ϊ6�����������м۲���ӶԸ���=�Ҽ�����+�µ��ӶԸ���=3+��5-3��1����1/2=4��VSEPRģ��Ϊ��������ṹ���ھ����У�Crԭ��λ�ڶ��㣬Cuԭ��λ������е㣬�þ�����Nԭ�Ӹ���=8��1/8=1��Cuԭ�Ӹ���=12��1/4=3����������mΪ244/NA�������ı߳�Ϊapm�����������Ϊ��apm��3=��a��10-10cm��3�����=m/V=![]() g/cm3��
g/cm3��

 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�����Ŀ��NH3��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863�ƻ������������н�ǿ��ѡ���ԣ���רһ�ԡ���֪��
��ӦI��4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) ��H=�D905.0 kJ��mol��1
4NO(g) +6H2O(g) ��H=�D905.0 kJ��mol��1
��Ӧ II��4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) ��H=��
2N2(g) +6H2O(g) ��H=��
��1��
��ѧ�� | H��O | O===O | N��N | N��H |
����kJ��mol��1 | a | b | c | d |
��H=__________________ ��
��2���ں��º���װ���г���һ������NH3��O2����ij�����������½��з�ӦI���������й���������ȷ����__________________��
A��ʹ�ô���ʱ���ɽ��÷�Ӧ�Ļ�ܣ��ӿ��䷴Ӧ����
B�������������4v��(NH3)=6v��(H2O)ʱ��˵����Ӧ�Ѵ�ƽ��
C����������n(NO)/n(NH3)=1ʱ��˵����Ӧ�Ѵ�ƽ��
��3����������ʱ�ᷢ����������������ӦI��II��Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1 mol NH3��2mol O2������й����ʵ�����ϵ����ͼ��
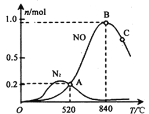
�ٸô����ڸ���ʱѡ��Ӧ____________ (� I ���� II������
��520��ʱ��4NH3(g)+5O2![]() 4NO(g) +6H2O(g)��ƽ�ⳣ��K=___________________ (��Ҫ��ó���������ֻ���г����ּ���ʽ����
4NO(g) +6H2O(g)��ƽ�ⳣ��K=___________________ (��Ҫ��ó���������ֻ���г����ּ���ʽ����
�����������NH3ת��ΪN2ƽ��ת���ʵĴ�ʩ��_______________
A��ʹ�ô���Pt/Ru
B��ʹ�ô���Cu/TiO2
C������NH3��O2�ij�ʼͶ�ϱ�
D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
E�����ͷ�Ӧ�¶�
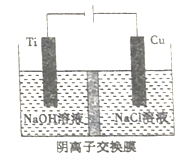
��4������Cu2O ���ھ��������Ĵ����ܶ��ܵ���ע����ҵ�ϳ��õ�ⷨCu2O���䷴ӦΪ2Cu+H2O![]() Cu2O+H2�� �������ӽ���Ĥ���Ƶ��Һ��OH-��Ũ�ȶ��Ʊ�����Cu2O��װ����ͼ��ʾ���������ϵĵ缫��ӦʽΪ___________________��������_______��Cu2Oʱ���ͻ���NA��������ͨ�����ӽ���Ĥ��
Cu2O+H2�� �������ӽ���Ĥ���Ƶ��Һ��OH-��Ũ�ȶ��Ʊ�����Cu2O��װ����ͼ��ʾ���������ϵĵ缫��ӦʽΪ___________________��������_______��Cu2Oʱ���ͻ���NA��������ͨ�����ӽ���Ĥ��