题目内容
【题目】化学键的键能是指气态原子间形成1 mol化学键时释放的能量。如H(g)+I(g)![]() H—I(g)放出297 kJ的能量,即H—I键的键能为297 kJ·mol-1,也可以理解为破坏1 mol H—I键需要吸收297 kJ的热量。下表是一些键能的数据(单位:kJ·mol-1)。
H—I(g)放出297 kJ的能量,即H—I键的键能为297 kJ·mol-1,也可以理解为破坏1 mol H—I键需要吸收297 kJ的热量。下表是一些键能的数据(单位:kJ·mol-1)。
共价键 | 键能 | 共价键 | 键能 | 共价键 | 键能 | 共价键 | 键能 |
H—H | 436 | Cl—Cl | 243 | H—Cl | 431 | H—O | 467 |
S | 255 | H—S | 339 | C—F | 427 | C—O | 358 |
C—Cl | 330 | C—I | 218 | H—F | 565 | N≡N | 945 |
回答下列问题:
(1)一个化学反应的反应热(设反应物、生成物均为气态)与反应物和生成物中的键能之间有密切的关系。由表中数据计算下列热化学方程式中的热效应:H2(g)+Cl2(g)![]() 2HCl(g) ΔH=____。
2HCl(g) ΔH=____。
(2)共价键的极性强弱对化学反应有很大的影响。卤代烃RX在同样条件下发生碱性水解反应(RX+NaOH![]() R—OH+NaX)时,RF、RCl、RBr、RI(R相同)的反应活性由小到大的顺序是_______。
R—OH+NaX)时,RF、RCl、RBr、RI(R相同)的反应活性由小到大的顺序是_______。
(3)根据表中数据判断CCl4的稳定性____(填“大于”或“小于”)CF4的稳定性。
(4)试预测C—Br键的键能范围(填具体数值):___<C—Br键的键能<____。
【答案】-183 kJ/mol RF<RCl<RBr<RI 小于 218kJ/mol 330kJ/mol
【解析】
(1)根据键能的定义,破坏1 mol H2(g)、 1molCl2(g)中的共价键分別需要消耗的能量为436 kJ、 243 kJ,而形成2mol HCl(g)中的共价键放出的能量为2×431kJ,总的结果是放出2×431kJ-(436kJ+243kJ)=183 kJ的能量,故H2(g)+Cl2(g)=2HCl(g)△H=-183 kJ/mol;
(2)从卤代烃发生碱性水解反应的化学方程式分析,发生水解反应时首先需要R-X键断裂,因此该键键能越大,越稳定,水解反应越不易发生,很显然稳定性的顺序是RF>RCl>RBr>RI,因此反应活性由小到大的顺序为RF<RCl<RBr<RI;
(3)键能:C-Cl键<C-F键,故稳定性:CCl4<CF4;
(4)Br的原子半径介于Cl与I之间,C- I键的键能(218kJ/mol)<C- Br键的键能<C-Cl键的键能(330kJ/mol)。

【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
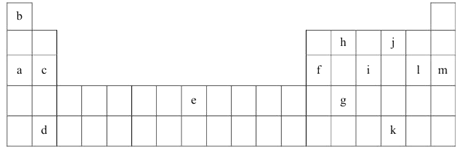
(1)上述元素的单质可能是电的良导体的是_______(填字母代号)。
(2)下表是一些气态原子的第一、二、三、四级电离能(kJ·mol-1):
锂 | X | Y | |
第一电离能 | 519 | 502 | 580 |
第二电离能 | 7296 | 4570 | 1820 |
第三电离能 | 11799 | 6920 | 2750 |
第四电离能 | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量:______________________________________。
②表中的Y可能为以上13种元素中的_________(填元素符号)元素,用元素符号表示X和j按原子个数1:1形成化合物的电子式___________________________。
(3)根据构造原理,用电子排布式表示e的核外电子排布式_______________。
(4)以上13种元素中,________(填元素符号)元素原子失去核外第一个电子需要的能量最多。
(5)a、e、f三种元素的最高价氧化物的水化物显碱性,其碱性最强的为_______(用化学符号作答)。f的氧化物具有两性,写出其与NaOH溶液反应的离子方程式___________________。