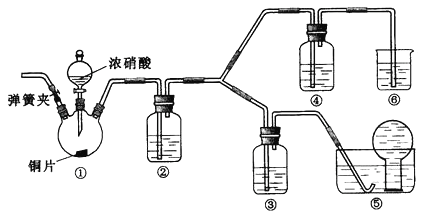
题目内容
【题目】回答下列问题:
(1)在一个恒温恒容的密闭容器中,可逆反应N2(g)+3H2(g)2NH3(g)
△H<0达到平衡的标志是(填编号)
①反应速率v(N2):v(H2):v(NH3)=1:3:2
②各组分的物质的量浓度不再改变
③体系的压强不再发生变化
④混合气体的密度不变
⑤单位时间内生成n mol N2的同时,生成3n mol H2
⑥2V(N2正)=V(NH3逆)
⑦单位时间内3mol H﹣H键断裂的同时2mol N﹣H键也断裂
⑧混合气体的平均相对分子质量不再改变
(2)现有八种物质:①干冰;②金刚石;③四氯化碳;④晶体硅;⑤过氧化钠;⑥碳化硅晶体;⑦溴化钠;⑧氖.请用编号填写下列空白:
A.属于原子晶体的是 , 其中熔点由高到低的顺序为
B.属于分子晶体的是 , 其中分子构型为正四面体的化合物的电子式为
C.既含有共价键又含有离子键的化合物是 , 其中阳离子个数与阴离子个数之比为 .
【答案】
(1)②③⑥⑧
(2)②④⑥;②⑥④;①③⑧;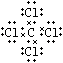 ;⑤;2:1
;⑤;2:1
【解析】解:(1)①速率之比等于对应物质的化学计量数之比,反应开始后一直成立,不能说明反应达到平衡状态,故①错误;②当体系达平衡状态时,反应混合物各组分的物质的量浓度不变,故②正确;③该反应正方向为计量数减小的反应,随着反应进行压强不断减小,当压强不变时,反应达到平衡状态,故③正确;④反应容器的体积不变,气体的质量守恒,所以密度始终不变,密度不变时不能说明反应达到平衡状态,故④错误;⑤单位时间内生成n mol N2表示逆速率,生成3n mol H2表示逆速率,都表示逆速率,不能说明反应达到平衡状态,故⑤错误⑥2V(N2正)=V(NH3逆),即氮气的正速率与氨气的逆速率之比等于计量数之比,则反应达到平衡状态,故⑥正确;⑦单位时间内3molH﹣H键断裂等效于6mol N﹣H键形成,同时6mol N﹣H键断裂,⑦错误;⑧混合气体的物质的量逐渐减小,质量不变,则平均相对分子质量逐渐增大,当平均相对分子质量不变时,即是平衡状态,故⑧正确;所以答案是:②③⑥⑧;(2)A.②金刚石、④晶体硅、⑥碳化硅是通过非极性键形成的原子晶体;②金刚石是熔点最高的晶体C﹣Si键长小于Si﹣Si,熔点:碳化硅>晶体硅;
所以答案是:②④⑥;②⑥④;B.①干冰是直线型分子,属于分子晶体;③四氯化碳是正四面体型分子晶体;⑧氖是由单原子分子构成的分子晶体四氯化碳的电子式为 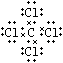 ;所以答案是:①③⑧;
;所以答案是:①③⑧; 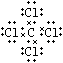 ;C.⑤过氧化钠既含有离子键,又含有非极性共价键,其阳离子个数与阴离子个数之比为2:1,所以答案是:⑤;2:1.
;C.⑤过氧化钠既含有离子键,又含有非极性共价键,其阳离子个数与阴离子个数之比为2:1,所以答案是:⑤;2:1.
【考点精析】解答此题的关键在于理解化学平衡状态的判断的相关知识,掌握状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等.

【题目】一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表如示。下列判断中正确的是
甲 | 乙 | 丙 | 丁 | ||
容器的体积/L | 2 | 2 | 2 | 1 | |
起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
SO2的平衡转化率% | 80 | α1 | α2 | α3 | |
A. 甲中反应的平衡常数小于乙 B. 该温度下,该反应的平衡常数K为400
C. SO2的平衡转化率:α1>α2=α3 D. 容器中SO3的物质的量浓度:丙=丁<甲