题目内容
【题目】常温下,向10 mL 1 mol/L HCl溶液中滴加等物质的量浓度的CH3COONa溶液。所得混合液的pH与加入CH3COONa溶液的体积(V)的变化如下图所示。下列说法不正确的是

A. 常温下,CH3COOH的电离常数约为2×10-5
B. 随着V的增加,混合液中水的电离程度先增加后减小
C. 当V=20mL时,混合液中c(Na+) >c(CH3COO-)> c(Cl-)>c(H+) >c(OH-)
D. 当混合液的pH=7时,混合液中c(CH3COOH)=c(Cl-)
【答案】B
【解析】A、当滴加的CH3COONa溶液体积为10 mL时,得到浓度均为0.5mol/L的CH3COOH和NaCl混合溶液,根据题中信息可知,此时溶液pH=2.5, c(CH3COO-)=c(H+)=10-2.5mol/L,c(CH3COOH)=0.5mol/L-10-2.5mol/L![]() 0.5mol/L,Ka=
0.5mol/L,Ka=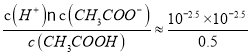 =2×10-5,选项A正确;B、酸和碱抑制水的电离,盐的水解促进水的电离,随着V的增加,混合溶液由盐酸转化为醋酸和氯化钠的混合溶液再到醋酸钠过量,混合液中水的电离程度逐渐增大,选项B不正确;C、当V=20mL时,混合液中以溶质为醋酸和醋酸钠按1:1形成的溶液,溶液呈酸性,说明醋酸的电离大于醋酸根离子的水解,c(Na+) =2 c(Cl-),2c(CH3COO-)>c(Na+),故有:c(Na+) >c(CH3COO-)> c(Cl-)>c(H+) >c(OH-),选项C正确;D、当混合液的PH=7时,①c(H+) =c(OH-),根据物料守恒有:②c(Na+) =c(CH3COO-)+ c(CH3COOH),根据电荷守恒有:③c(H+)+c(Na+) =c(CH3COO-)+ c(OH-) +c(Cl-),将①②式代入③式可得c(CH3COOH)=c(Cl-),选项D正确。答案选B。
=2×10-5,选项A正确;B、酸和碱抑制水的电离,盐的水解促进水的电离,随着V的增加,混合溶液由盐酸转化为醋酸和氯化钠的混合溶液再到醋酸钠过量,混合液中水的电离程度逐渐增大,选项B不正确;C、当V=20mL时,混合液中以溶质为醋酸和醋酸钠按1:1形成的溶液,溶液呈酸性,说明醋酸的电离大于醋酸根离子的水解,c(Na+) =2 c(Cl-),2c(CH3COO-)>c(Na+),故有:c(Na+) >c(CH3COO-)> c(Cl-)>c(H+) >c(OH-),选项C正确;D、当混合液的PH=7时,①c(H+) =c(OH-),根据物料守恒有:②c(Na+) =c(CH3COO-)+ c(CH3COOH),根据电荷守恒有:③c(H+)+c(Na+) =c(CH3COO-)+ c(OH-) +c(Cl-),将①②式代入③式可得c(CH3COOH)=c(Cl-),选项D正确。答案选B。
