题目内容
【题目】下列实验设计不合理的是
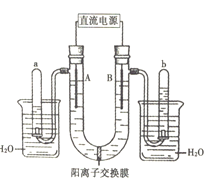
A. 自制“84”消毒液
自制“84”消毒液
B.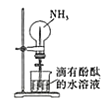 利用喷泉实验探究NH3的部分性质
利用喷泉实验探究NH3的部分性质
C. 制备Fe(OH)2白色沉淀
制备Fe(OH)2白色沉淀
D.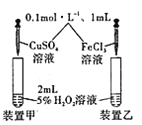 探究不同催化剂对双氧水分解速率的影响
探究不同催化剂对双氧水分解速率的影响
【答案】A
【解析】
A. A为密闭电解饱和食盐水装置,生成的氯气和氢氧化钠反应,但生成的氢气没办法排出,有安全隐患,故A错误;
B.NH3及易溶于水,且氨水显碱性,所以可以利用滴有酚酞的水进行喷泉实验探究NH3的部分性质,故B正确;
C.因为Fe(OH)2非常不稳定,在空气中就容易被氧化生成Fe(OH)3红褐色沉淀,所以制备Fe(OH)2时一定要隔绝空气,故C正确;
D.由装置图可知,两只试管加入相同浓度和体积的双氧水,加入的催化剂不同,反应放出氧气的速率不同,故D正确;
故答案:A。

练习册系列答案
相关题目