��Ŀ����
��16�֣�������и��⣺
��K2Cr2O7����ɫ����Cr2(SO4)3����ɫ����K2SO4��H2SO4��C2H5OH��CH3COOH��H2O�ֱ�����ͬһ������ԭ��Ӧ�еķ�Ӧ���������÷�Ӧԭ���������ڼ��˾���Ƿ�ƺ���
����˾���ƺ������������������ʾ�� ɫ��
��д������ƽ�÷�Ӧ�Ļ�ѧ����ʽ�� ��
������ڷ�Ӧ������1mol�������ת�Ƶĵ�������Ϊ ��
���������ϰ�װ��Ч��ת��������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯����������Ӧ�����������ʣ���������β����Ⱦ��
��֪��N2(g)+ O2(g)="2NO(g) " ��H=+180. 5 kJ/mol [��Դ:ѧ*��*��]
5 kJ/mol [��Դ:ѧ*��*��]
2C(s)+ O2(g)="2CO(g) " ��H=��221.0 kJ/mol
C(s)+ O2(g)=CO2(g) ��H=��393.5 kJ/mol
��β��ת���ķ�Ӧ֮һ��2NO(g)+2CO(g)=N2(g)+2CO2(g) ��H �� ��
��Ϊ�����β��ת���ķ�Ӧ�����ʺ�NO��ת���ʣ���ȡ����ȷ��ʩΪ ��
| A���Ӵ���ͬʱ�����¶� | B���Ӵ���ͬʱ����ѹǿ |
| C�������¶�ͬʱ����N2 | D�������¶�ͬʱ����ѹǿ |
����֪NH4A��ҺΪ���ԣ���֪��HA��Һ�ӵ�Na2CO3��Һ��������ų������ƶϣ���(NH4)2CO3��Һ��pH 7���������������
����ͬ�¶��£������ʵ���Ũ�ȵ�������������Һ��pH�ɴ�С������˳��Ϊ
 ��������ţ�
��������ţ�a��NH4HCO3 b��NH4A c��(NH4)2CO3 d��NH4Cl
��16�֣�
�Ţ���ɫ��1�֣�
��2K2Cr2O7 + 3C2H5OH + 8H2SO4 ��2Cr2(SO4)3 + 3CH3COOH + 2K2SO4 + 11H2O ��3�֣�
��2.408��1024��4NA��2�֣�
�Ƣ٣�746.5 kJ/mol ��2�֣� ��B��2�֣��� ������С��2�֣�
�� �٣���2�֣� ��c��a��b��d��2�֣�
����


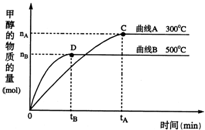 ���ý�̿����Ȼ����ȡ���۵�CO��H2�������ڰ��ϳɺ��л��ϳ���Ŀǰ��ҵ��������Ҫ;����
���ý�̿����Ȼ����ȡ���۵�CO��H2�������ڰ��ϳɺ��л��ϳ���Ŀǰ��ҵ��������Ҫ;����