题目内容
(2012?河北模拟)如图所示为常见气体制备、干燥、性质验证和尾气处理的部分仪器装置,请根据要求完成下列各题,仪器装置可任意选用,必要时可重复选择.
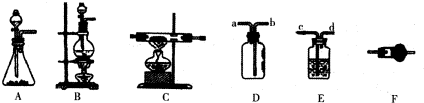
(1)实验室需要制备少量Cl2,可以选用装置
(2)某学习小组要完成“氨的催化氧化”实验,他们从上述仪器中选择了一部分,并按气流方向从左到右连接顺序为A→F→C→D→E,请写出C中氨的催化氧化反应的化学方程式
①若要通过A装置得到两种气体,则锥形瓶中的固体是
②装置F的作用是
③装置D中的现象是

(1)实验室需要制备少量Cl2,可以选用装置
A
A
或B
B
(填仪器编号),发生的化学方程式2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
或MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
,Cl2有毒,其尾气吸收装置可选用E或F,那么E中液体是
| ||
NaOH溶液
NaOH溶液
,F中的物质是碱石灰
碱石灰
.(2)某学习小组要完成“氨的催化氧化”实验,他们从上述仪器中选择了一部分,并按气流方向从左到右连接顺序为A→F→C→D→E,请写出C中氨的催化氧化反应的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
①若要通过A装置得到两种气体,则锥形瓶中的固体是
Na2O2
Na2O2
(填化学式),分渡漏斗中盛装浓氨水
浓氨水
(填名称).②装置F的作用是
干燥气体除去氨气和氧气中的水蒸气
干燥气体除去氨气和氧气中的水蒸气
,装置C中固体的作用是催化作用
催化作用
.③装置D中的现象是
有红棕色气体生成
有红棕色气体生成
,从实验安全的角度考虑,气流的方向是a进
进
b出
出
(填“进”或“出”).分析:(1)依据实验室制氯气的反应原理书写,一般用二氧化锰和浓盐酸加热反应,常温下可以用高锰酸钾和浓盐酸反应制的;氯气有毒不能排放到大气中,需要用氢氧化钠溶液吸收尾气,或用固体碱石灰吸收;
(2)氨气的催化氧化反应生成一氧化氮和水;
①若要通过A装置得到两种气体,要求是锥形瓶内的固体和分液漏斗中的液体常温下发生反应生成两种气体,则锥形瓶中的固体是判断为过氧化钠,分液漏斗中是氨水,滴入后生成氨气和氧气;
②装置B是干燥管主要是利用固体对气体进行干燥、除杂,装置C中是氨气的催化氧化反应玻璃管中 固体是催化剂;
③装置D中生成的一氧化氮和空气中的氧气反应生成红棕色的二氧化氮气体,从实验安全的角度考虑,为防止倒吸可以使导气管短进长出.
(2)氨气的催化氧化反应生成一氧化氮和水;
①若要通过A装置得到两种气体,要求是锥形瓶内的固体和分液漏斗中的液体常温下发生反应生成两种气体,则锥形瓶中的固体是判断为过氧化钠,分液漏斗中是氨水,滴入后生成氨气和氧气;
②装置B是干燥管主要是利用固体对气体进行干燥、除杂,装置C中是氨气的催化氧化反应玻璃管中 固体是催化剂;
③装置D中生成的一氧化氮和空气中的氧气反应生成红棕色的二氧化氮气体,从实验安全的角度考虑,为防止倒吸可以使导气管短进长出.
解答:解:(1)一般用二氧化锰和浓盐酸加热反应,常温下可以用高锰酸钾和浓盐酸反应制,则选择A或B,常温下可以用高锰酸钾和浓盐酸反应制取氯气的反应化学方程式为2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;用二氧化锰和浓盐酸加热反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;氯气有毒不能排放到大气中,需要用氢氧化钠溶液吸收尾气,或用固体碱石灰吸收,
故答案为:A;B;2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;NaOH溶液;碱石灰;
(2)氨气的催化氧化反应生成一氧化氮和水;反应的化学方程式为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
①若要通过A装置得到两种气体,要求是锥形瓶内的固体和分液漏斗中的液体常温下发生反应生成两种气体,则锥形瓶中的固体是判断为过氧化钠,分液漏斗中是氨水,滴入后生成氨气和氧气,故答案为:Na2O2;浓氨水;
②装置F是干燥管主要是利用固体对气体进行干燥、除杂,除去氨气和氧气中的水蒸气;装置C中是氨气的催化氧化反应玻璃管中固体是催化剂,故答案为:干燥气体除去氨气和氧气中的水蒸气;催化作用;
③装置D中生成的一氧化氮和空气中的氧气反应生成红棕色的二氧化氮气体,从实验安全的角度考虑,为防止倒吸可以使导气管短进长出;故答案为:红棕色气体生成;进;出.
| ||
故答案为:A;B;2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;MnO2+4HCl(浓)
| ||
(2)氨气的催化氧化反应生成一氧化氮和水;反应的化学方程式为:4NH3+5O2
| ||
| △ |
| ||
| △ |
①若要通过A装置得到两种气体,要求是锥形瓶内的固体和分液漏斗中的液体常温下发生反应生成两种气体,则锥形瓶中的固体是判断为过氧化钠,分液漏斗中是氨水,滴入后生成氨气和氧气,故答案为:Na2O2;浓氨水;
②装置F是干燥管主要是利用固体对气体进行干燥、除杂,除去氨气和氧气中的水蒸气;装置C中是氨气的催化氧化反应玻璃管中固体是催化剂,故答案为:干燥气体除去氨气和氧气中的水蒸气;催化作用;
③装置D中生成的一氧化氮和空气中的氧气反应生成红棕色的二氧化氮气体,从实验安全的角度考虑,为防止倒吸可以使导气管短进长出;故答案为:红棕色气体生成;进;出.
点评:本题考查了实验室制气体的反应装置选择,反应原理的判断应用,主要考查氯气的制备方法和装置选择,氨气的催化氧化,污染气体的处理方法,气体除杂的装置选择应用,掌握实验基本操作是解题关键.

练习册系列答案
相关题目
 (2012?河北模拟)短周期金属元素甲~戊在元素周期表中的相对位置如图所示,下列判断不正确的是( )
(2012?河北模拟)短周期金属元素甲~戊在元素周期表中的相对位置如图所示,下列判断不正确的是( ) (2012?河北模拟)氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )
(2012?河北模拟)氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )