题目内容
2.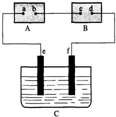 图中A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,e、f为铂电极.接通电路后,发现B上的c点显红色.试回答:
图中A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,e、f为铂电极.接通电路后,发现B上的c点显红色.试回答:(1)电源A上的b为负极.
(2)d极的电极反应式是2Cl--2e-=Cl2↑;.B上总反应的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(3)e、f电极上所产生的气体及体积比是V (O2):V (H2)=1:2.
分析 A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,发现c点显红色,则c点发生2H++2e-=H2↑,所以c为阴极,电源上b为负极,根据电解池的工作原理以及电极反应式来计算回答即可.
解答 解:(1)发现c点显红色,则c点发生2H++2e-=H2↑,所以c为阴极,电源上b为负极,故答案为:负;
(2)c为阴极,d是阳极,电解氯化钠溶液时d点发生2Cl--2e-=Cl2↑;电解氯化钠溶液的总的化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:2Cl--2e-=Cl2↑;2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(3)e、f 各极的电极反应式分别为4OH--4e-=2H2O+O2↑,2H++2e-=H2↑,据电子守恒可知,各极的电解产物的物质的量之比为1﹕2,即:V (O2):V (H2)=1:2
故答案为:V (O2):V (H2)=1:2.
点评 本题考查电解原理,明确c点显红色是解答本题的突破口,熟悉发生的电极反应即可解答,题目难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
13.NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 常温常压下,7.1gCl2含有的Cl2分子数为0.2NA | |
| B. | 0.1 mol羟基(-OH)含有的电子数为NA | |
| C. | 1.7gNH3含有的电子数为NA | |
| D. | 标准状况下,11.2LSO3中含有的氧原子数为1.5NA |
10.下列关于铜电极的叙述中不正确的是( )
| A. | 铜锌原电池中铜是正极 | |
| B. | 用电解法电解氯化钠溶液时,铜可作阴极 | |
| C. | 用电解法精炼粗铜时粗铜作阴极 | |
| D. | 在镀件上电镀铜时可用金属铜作阳极 |
17.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 0.1mol•L-1稀硫酸100mL中含有硫酸根个数为0.1NA | |
| B. | 1molC10H22分子中共价键总数为31NA | |
| C. | 7.1g氯气与足量的NaOH溶液反应,转移电子数为0.2NA | |
| D. | 9g重水中所含有的电子总数为5NA |
14.下列事故处理不正确的是( )
| A. | 将一氧化碳中毒者移到通风处抢救 | |
| B. | 眼睛里不慎溅进了药液,应立即用水冲洗,并且用手使劲揉眼睛 | |
| C. | 不慎将浓硫酸溅到皮肤上,应立即用大量水冲洗 | |
| D. | 不慎碰倒酒精灯,洒出的酒精在桌上燃烧时,应立即用湿抹布扑盖 |