题目内容
8.四氯化锡是无色液体,熔点-33“C,沸点114℃.氯气与金属锡在加热时反应可以用来制备SnCl4,SnCl4极易水解,在潮湿的空气中发烟.实验室可以通过题1O图装置制备少量SnCl4 (夹持装置略).
(1)仪器C的名称为蒸馏烧瓶;
(2)装置Ⅰ中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(3)装置Ⅱ中的最佳试剂为饱和氯化钠溶液,装置Ⅶ的作用为防止空气中水蒸气进入Ⅵ中,SnCl4水解;
(4)若装置连接顺序为Ⅰ-Ⅱ一Ⅳ一Ⅴ一Ⅵ一Ⅶ,在Ⅳ中除生成SnCl4外,还会生成的含锡的化合物的化学式为.
(5)Ⅳ中加热的作用之一是促进氯气与锡粉反应,加热的另一作用为;
(6)若Ⅳ中用去锡粉11.9g,反应后,Ⅵ中锥形瓶里收集到23.8g SnCl4,则SnCl4的产率为.
分析 由装置图可知装置Ⅰ应为制备氯气装置,涉及离子反应为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,装置Ⅱ为饱和食盐水,装置Ⅲ为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅳ中反应生成SnCl4,经冷却后在装置Ⅵ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅵ中,以此解答该题.
(1)认识常见的化学实验仪器
(2)A为制备氯气装置,在加热条件下进行,应为浓盐酸和二氧化锰的反应
(3)B为饱和食盐水,C为浓硫酸,氯气经除杂,干燥后与锡在D中反应生成SnCl4,因SnCl4极易水解,F可起到防止空气中的水蒸气进入E中
(4)若没有III,则SnCl4会水解产生Sn(OH)4
(5)加热促进SnCl4气化,便于分离
(6)Sn+2Cl2=△=SnCl4,11.9gSn即0.1mol完全反应可生成SnCl426.1g,故产率为23.8/26.1×100%=91.2%
解答 解:由装置图可知装置Ⅰ应为制备氯气装置,涉及离子反应为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,装置Ⅱ为饱和食盐水,装置Ⅲ为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅳ中反应生成SnCl4,经冷却后在装置Ⅵ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅵ中.
(1)仪器C的名称为蒸馏烧瓶,故答案为:蒸馏烧瓶;
(2)装置Ⅰ中浓盐酸与MnO2在加热时发生反应产生氯气.发生反应的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(3)由于盐酸有挥发性,所以在制取的氯气中含有杂质HCl,在与金属锡反应前要除去,因此装置Ⅱ中的最佳试剂为除去HCl同时还可以减少氯气消耗的饱和食盐水;SnCl4极易水解,在潮湿的空气中发烟.为了防止盐水解,所以要防止起水解.装置Ⅶ的作用为防止空气中的水蒸气进入Ⅵ中使SnCl4水解,
故答案为:饱和氯化钠溶液;防止空气中水蒸气进入Ⅵ中,SnCl4水解;
(4)未反应的氯气没有除去,缺少尾气处理装置,故答案为:缺少尾气处理装置;
(5)如果没有装置Ⅲ,则在氯气中含有水蒸汽,所以在Ⅳ中除生成SnCl4外,还会生成SnCl4水解产生的含锡的化合物Sn(OH)4或SnO2,故答案为:Sn(OH)4或SnO2等;
(6)若Ⅳ中用去锡粉11.9g,则n(Sn)=0.1mol,理论上产生的SnCl4的物质的质量是m(SnCl4)=0.1mol×261g/mol=26.1g所以反应后,若Ⅵ中锥形瓶里收集到23.8gSnCl4,则SnCl4的产率为$\frac{23.8g}{26.1g}$×100%=91.2%,故答案为:91.2%.
答案解析
点评 本题考查物质的制备,涉及仪器的识别、氯气的实验室制取方法、实验操作的目的、盐的水解、物质产率的计算等知识,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力的考查,注意把握题给信息,结合物质的性质设计实验步骤,题目难度不大.

 初中学业考试导与练系列答案
初中学业考试导与练系列答案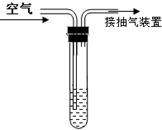 二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:| 级别 | 一级指标 | 二级指标 | 三级指标 |
| 浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
(1)将含碘(I2)1.27mg的碘溶液加入到试管中;
(2)向试管内滴加2~3滴淀粉溶液,溶液显蓝色(淀粉遇I2便蓝)
(3)通过抽气装置抽气,使空气由导气管进入试管与碘溶液接触.
(4)当溶液由蓝色变为无色时,测定通过空气的总量为1m3请你通过计算判断,该地区空气中二氧化硫的浓度级别.
 ,它不稳定,在水中易发生岐
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如表:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
回答下列问题:
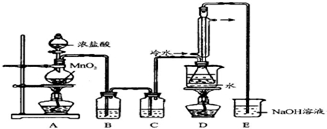
(1)写出A装置中发生反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.
(3)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中ACD实验.
A.石油分馏 B.制备乙烯 C.制取乙酸乙酷 D.制取溴苯
(4)B装置中盛放的是饱和食盐水,反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏,D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化.
(5)A装置仪器装配时,整套装置装配完毕后,应先进行气密性检查,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是防止倒吸.
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清,出现该现象的原因可用化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.实验完毕,当把剩余浓盐酸倒人E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是ClO-+2H++Cl-=Cl2↑+H2O.(用离子方程式表示)



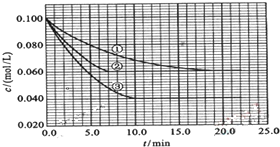 浓度为0.06mol/L.
浓度为0.06mol/L.