��Ŀ����
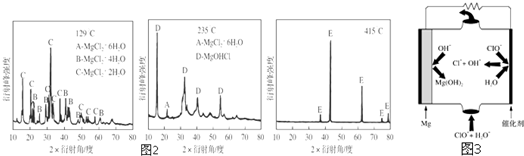
3��ʵ���Ҳ���MgCl2��AlCl3�Ļ����Һ�������ˮ��Ӧ�Ʊ�MgAl2O4����Ҫ����ͼ1��
��1����ͼ2��ʾ�����˲����е�һ��������©���¶˼���δ�����ձ��ڱڣ�
��2���ж������г����Ƿ�ϴ�����õ��Լ���AgNO3��Һ���������ữ��AgNO3��Һ�������±���ʱ������ʢ�Ź��������������������
��3����ˮAlCl3��183������������ʪ��������������������ʵ���ҿ���ͼ3װ���Ʊ���

д��Aװ���е����ӷ�ӦMnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��װ��B��ʢ�ű���NaCl��Һ����װ�õ���Ҫ�����dz�ȥ�����е��Ȼ��⣮F���Լ��������Ƿ�ֹ����������Һ�е�ˮ����Eװ�ã���һ������װ���ʵ��Լ���Ҳ����F��G�����ã���װ����Լ�Ϊ��ʯ�ң�
��4��Cl2��Ca��OH��2��ȡƯ�۾��Ļ�ѧ����ʽ��2Ca��OH��2+2Cl2�TCaCl2+Ca��ClO��2+2H2O��
��5��ʵ�鳣��������Na2SO3��Һ���ն�����������д����Ӧ�����ӷ�Ӧ����ʽ��SO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
���� ��1��Ϊ�˷�ֹҺ�彦�����ڹ���ʱӦ�ý�©���ļ��첿�ֽ����ձ����ڱڣ�
��2�����������֪��������Ӧ�ø��������Ӻ�笠����ӣ����ж��Ƿ�ϴ��������ȡ�������һ��ϴ��Һ�����������ữ����������Һ�����жϣ������ɰ�ɫ��������˵��û��ϴ�Ӹɾ�����û�г������ɣ���˵���Ѿ�ϴ�Ӹɾ���
��3����ͼ3װ���Ʊ��Ȼ���ʱ������Ũ���������������A�з�Ӧ���������������Ȼ����ӷ��������Ƶõ����������Ȼ����ˮ������B�зű���NaCl��Һ����ȥ�����е��Ȼ��⣬C����Ũ���������ɵ��Ȼ�����ˮ�⣬��Ӧ��β��Ϊ������������������������������E��G֮���Fװ���з�Ũ�����ֹ����������Һ�е�ˮ����Eװ�ã�F��G������������������ˮ�������ü�ʯ�Ҵ��棬�ݴ˴��⣻
��4��Cl2��Ca��OH��2��Ӧ�����Ȼ��ƺʹ�����ƣ�
��5��Na2SO3��Һ����������������ԭ��Ӧ������������Ӻ������ӣ����ݵ���غ��Ԫ���غ���д���ӷ���ʽ��
��� �⣺��1������ʱӦ�ý�©���ļ��첿�ֽ����ձ����ڱڣ���ֹҺ�彦����
�ʴ�Ϊ��©���¶˼���δ�����ձ��ڱڣ�
��2��������Ӧ�ø��������Ӻ�笠����ӣ����ж��Ƿ�ϴ��������ȡ�������һ��ϴ��Һ������AgNO3��Һ���������ữ��AgNO3��Һ����Һ�����жϣ������ɰ�ɫ��������˵��û��ϴ�Ӹɾ�����û�г������ɣ���˵���Ѿ�ϴ�Ӹɾ������±��չ���Ӧ�������н��У�
�ʴ�Ϊ��AgNO3��Һ���������ữ��AgNO3��Һ����������
��3����ͼ3װ���Ʊ��Ȼ���ʱ������Ũ���������������A�з�Ӧ������������Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O�������Ȼ����ӷ��������Ƶõ����������Ȼ����ˮ������B�зű���NaCl��Һ����ȥ�����е��Ȼ��⣬C����Ũ���������ɵ��Ȼ�����ˮ�⣬��Ӧ��β��Ϊ������������������������������E��G֮���Fװ���з�Ũ�����ֹ����������Һ�е�ˮ����Eװ�ã�F��G������������������ˮ�������ü�ʯ�Ҵ��棬
�ʴ�Ϊ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O����ȥ�����е��Ȼ��⣻��ֹ����������Һ�е�ˮ����Eװ�ã���ʯ�ң�
��4��Cl2��Ca��OH��2��Ӧ�����Ȼ��ƺʹ�����ƣ���Ӧ�ķ���ʽΪ2Ca��OH��2+2Cl2�TCaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Ca��OH��2+2Cl2�TCaCl2+Ca��ClO��2+2H2O��
��5��Na2SO3��Һ����������������ԭ��Ӧ������������Ӻ������ӣ���Ӧ�����ӷ���ʽΪSO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
�ʴ�Ϊ��SO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
���� ���⿼�����ʵ��Ʊ�ʵ����ƣ���Ŀ�ѶȲ���ע�����ʵ����Ƶ���������˳�����ʵ��ԭ����

���и������ӻ�����ܴ������棬��������Ӧ�Լ���ᷢ����ѧ�仯���ҷ�����Ӧ�����ӷ���ʽ��д������ȷ����
ѡ�� | ������ | �����Լ� | �����Լ�������Ӧ�����ӷ���ʽ |
A | Na����Fe3����Cl����I�� | NaOH��Һ | Fe3��+3OH��=Fe(OH)3�� |
B | Mg2����HCO | ����NaOH��Һ | Mg2����HCO H2O��Mg(OH)2����CO |
C | K����NH3��H2O��CO | ͨ������CO2 | 2OH����CO2=CO |
D | Na����NO | NaHSO4��Һ | SO |
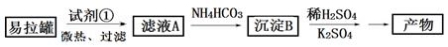
 ���Ŵ�����Ⱦ���������أ��������ڡ�ʮ���塱�ڼ䣬����������SO2���ŷ�������8%���������NOx���ŷ�������10%��Ŀǰ������������Ⱦ�ж��ַ�����
���Ŵ�����Ⱦ���������أ��������ڡ�ʮ���塱�ڼ䣬����������SO2���ŷ�������8%���������NOx���ŷ�������10%��Ŀǰ������������Ⱦ�ж��ַ�������1����CH4����ԭ��������������������������Ⱦ����֪��
��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ•mol-1
��CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ•mol-1
��H2O��g���TH2O��l����H=-44.0kJ•mol-1
д��CH4��g����NO2��g����Ӧ����N2 ��g����CO2 ��g����H2O��1�����Ȼ�ѧ����ʽCH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g����H=-955kJ•mol-1��
��2������Fe2+��Fe3+�Ĵ����ã������¿ɽ�SO2ת��ΪSO42-���Ӷ�ʵ�ֶ�SO2����������֪��SO2�ķ���ͨ�뺬Fe2+��Fe3+����Һʱ������һ����Ӧ�����ӷ���ʽΪ4Fe2++O2+4H+�T4Fe3++2H2O������һ��Ӧ�����ӷ���ʽΪ2Fe3++SO2+2H2O=2Fe2++SO42-+4H+��
��3���û���̿��ԭ��������������йط�ӦΪ��C��s��+2NO��g��?N2 ��g��+CO2 ��g����ij�о�С�����ܱյ���������У���������������䣬��������������Բ��ƣ�����NO�������Ļ���̿�����£�T1�棩�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
Ũ��/mol•L-1 ʱ��/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
�ڸ��ݱ������ݣ�����T1��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ0.56��������λС������
��һ���¶��£�����NO����ʼŨ��������NO��ƽ��ת���ʲ��䣨����������䡱��С������
�����и�������Ϊ�жϸ÷�Ӧ�ﵽƽ�����CD���������ĸ����
A��������ѹǿ���ֲ��䡡�� B�� 2v����NO��=v����N2��
C��������CO2������������� D�����������ܶȱ��ֲ���
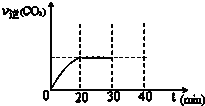
��30minĩ�ı�ijһ��������һ��ʱ�䷴Ӧ���´ﵽƽ�⣬��ı�����������Ǽ�СCO2 ��Ũ�ȣ�����ͼ�л���30min��40min�ı仯���ߣ�
 ��
�� Si+CO2��
Si+CO2�� .��Mg(HCO3)2��Һ�м������ռ���Һ:Mg2��+2HCO3��+2OH��=MgCO3��+2H2O+CO32��
.��Mg(HCO3)2��Һ�м������ռ���Һ:Mg2��+2HCO3��+2OH��=MgCO3��+2H2O+CO32��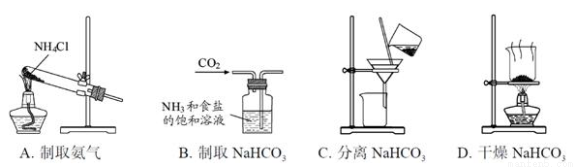
 ��Cl��
��Cl��
 ��SO
��SO