��Ŀ����
����Ŀ�����н�����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ����ȷ���ǣ� ��
A.��ҵ�Ͽɽǵ�ⷨ�Ʊ�Mg��MgCl2�����ڣ� ![]() Mg+C12��
Mg+C12��
B.��FeSO4��ȥ���Է�ˮ�е�Cr2O72����Cr2O72��+Fe2++14H+�T2Cr3++Fe3++7H2O
C.��CaSO4�����μ�أ�CaSO4��s��+Na2CO3��aq��?CaCO3��s��+Na2SO4��aq��
D.��Ca��ClO��2��Һ��ͨ������CO2��Ca2++2ClO��+H2O+CO2�T2HClO+CaCO3��
���𰸡�B
���������⣺A����ҵ�Ͽɽǵ�ⷨ�Ʊ�Mg����Ӧ�Ļ�ѧ����ʽΪ��MgCl2�����ڣ� ![]() Mg+C12������A��ȷ��
Mg+C12������A��ȷ��
B����FeSO4��ȥ���Է�ˮ�е�Cr2O72�� �� ���߷���������ԭ��Ӧ����ȷ�����ӷ���ʽΪ��Cr2O72��+6Fe2++14H+�T2Cr3++6Fe3++7H2O����B����
C����CaSO4�����μ�أ�̼����ת����̼��Ƴ�������Ӧ�Ļ�ѧ����ʽΪ��CaSO4��s��+Na2CO3��aq��CaCO3��s��+Na2SO4��aq������C��ȷ��
D����Ca��ClO��2��Һ��ͨ������CO2 �� ��Ӧ���ɴ������̼��Ƴ�������Ӧ�����ӷ���ʽΪ��Ca2++2ClO��+H2O+CO2�T2HClO+CaCO3������D��ȷ��
��ѡB��

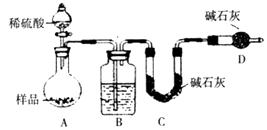
����Ŀ���о������к������Ҫ��SO2��H2S����ת���Ի�������������Ҫ���壮
��1��SO2�Ĵ����ŷŻ��������صĻ��������� �� ��ʪ�����£�д��������SO2ת��ΪHSO3���ķ���ʽ ��
��2�������е�����ɽ�������H2S��������Ӧ������SO42�� �� ������Ӧ�������仯ʾ��ͼ1���£�
1mol H2S��g��ȫ��������SO42����aq�����Ȼ�ѧ����ʽΪ
��3��SO2�ǹ�ҵ�������ԭ������֮һ��һ���¶��£����ݻ�Ϊ2L���ܱ������г���һ������SO2��O2 �� ������Ӧ��2SO2��g��+O2��g��2SO3��g���������вⶨ�IJ������ݼ�����
ʱ��/min | n��SO2��/mol | n��O2��/mol |
0 | 0.10 | 0.050 |
4 | 0.050 | 0.025 |
5 | 0.040 | |
8 | 0.020 |
�ٷ�Ӧ��0��4min�ڵ�ƽ������Ϊv��SO2��=��
�ڴ��¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K= ��
��8minʱ��ά���¶Ȳ��䣬����Ӧ��������ͨ��0.020mol SO2��g����0.010mol O2��g�������´ﵽƽ��ʱ���������SO2�İٷֺ����������С�����������䡱������4����H2S �Ϳ����Ļ������ͨ��FeCl3��FeCl2��CuCl2�Ļ����Һ�з�Ӧ����S��������ת����ͼ2��ʾ��
�����¶�һ���Ͳ�������Һ�������£�����ͨ�������壬����ֽ��裮��ʹ���ɵ������в���CuS���ɲ�ȡ�Ĵ�ʩ�� ��
��һ����˵�����һ����Ӧ��ƽ�ⳣ������105 �� ͨ����Ϊ��Ӧ���еý���ȫ���෴�����һ����Ӧ��ƽ�ⳣ��С��10��5 �� ����Ϊ�����Ӧ���ѽ��У���֪�����¸����ʵ��ܶȻ�������ƽ�ⳣ����
CuS��Ksp=6.3��10��36��H2S��K a1=1.3��10��7 �� K a2=7.1��10��15 ��
ͨ������˵����ӦCuS��s��+2H+ ��aq��=Cu2+��aq��+H2S��aq�����еij̶� �� 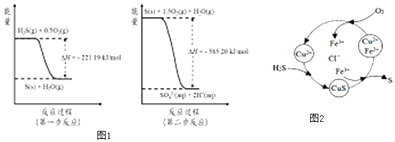
����Ŀ����֪���Ҷ����׳Ʋ��ᣨ�ṹ��ʽΪHOOC��COOH���ɼ�дΪH2C2O4)��25��ʱ������ĵ���ƽ�ⳣ��ΪK1=5.0��10-2��K2=5.4��10-5��̼�ᣨH2CO3���ĵ���ƽ�ⳣ��ΪK1=4.5��10-7��K2= 4.7��10-11������Ƶ�Ksp=4.0��10-8��̼��Ƶ�Ksp=2.5��10-9���ش��������⣺
��1����ͬ�����µ����ʵ���Ũ�ȵ�Na2C2O4��Һ��pH��Na2CO3��Һ��pH_____ ��������������С���������������
��2�������½�20 mL 0.4 mol/L��KOH��Һ��20 mL 0.2 mol/L�IJ�����Һ��ϣ����Ϻ���Һ��������Ũ�ȵĴ�С˳��Ϊ_______________________��
��3��25��ʱ��20 mL̼��Ƶı�����Һ����μ���8.0��10-4 mol/L�IJ������Һ20 mL���ܷ��������________����������������������.
��4������KMnO4��Һ���������H2C2O4����Һ��Ӧ��ij̽��С�����÷�Ӧ��������Һ��ɫ��ʧ�����ķ������о�Ӱ�췴Ӧ���ʵ����ء�
��.ʵ��ǰ������Ũ��Ϊ0.1000molL-1����KMnO4����Һ�ζ�δ֪Ũ�ȵIJ��ᡣ
�ٸ��������Һ����______������ϡ����������ϡ����������ϡ���������ữ��д���ζ������з�����Ӧ�����ӷ���ʽ _____________________________��
���ζ������в����ζ��ܵ�ͼʾ��ȷ���� ______________����������
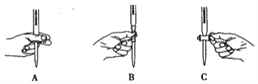
���жϵζ��յ�ķ����ǣ�_________________________________________��
������������KMnO4����Һʱ,��������ƿ�Ŀ̶��ߣ���ʹ��õIJ�����ҺŨ��________������ƫ��������ƫ������������������
��.ͨ���ζ�ʵ��õ�������Һ��Ũ��Ϊ0.2000mol��L-1 ���øò�����Һ���±����к���ʵ�飨ÿ��ʵ�������Һ��������Ϊ8mL����
ʵ���� | �� �ȣ����� | ��������(g) | ���Ը��������Һ | ʵ��Ŀ�� a.ʵ��1��2̽�� b.ʵ��1 ��3 ̽����Ӧ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죻 c.ʵ��1 ��4 ̽�������Ը÷�Ӧ���ʵ�Ӱ�졣 | |
�����mL�� | Ũ�� (molL-1) | ||||
1 | 25 | 0.5 | 4 | 0.1000 | |
2 | 50 | 0.5 | 4 | 0.1000 | |
3 | 25 | 0.5 | 4 | 0.0100 | |
4 | 25 | 0 | 4 | 0.1000 | |
��д������a ��Ӧ��ʵ��Ŀ��_______________________��
�ڸ�С��ͬѧ��ʵ��1��3�ֱ����������ʵ�飬�������ʵ�����ݣ��ӻ�����ȿ�ʼ��ʱ����
ʵ���� | ��Һ��ɫ����ʱ�䣨min�� | ||
��1 �� | ��2 �� | ��3 �� | |
1 | 14.0 | 13.0 | 11.0 |
3 | 6.5 | 6.7 | 6.8 |
�����������ݺ�ó���������������ͬʱ�����Ը��������Һ��Ũ��ԽС����ɫʱ���Խ�̣�����Ӧ���ʾ�Խ�����Ľ��ۡ�ijͬѧ��Ϊ��С����̽����Ӧ��Ũ�ȶ�����Ӱ������ʵ�鷽������д������⣬�Ӷ��õ��˴����ʵ����ۣ�������Ľ���ʵ�鷽��________��