题目内容
氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如图所示:
(1)该流程中可以循环的物质是 。
(2)电解法制碱的主要原料是饱和食盐水,由 于粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式 ,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果 。
(3)如图是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成)。则B处产生的气体是 , E电极的名称是 。电解总反应的离子方程式为 。
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为 。
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3,电解槽的电流强度1.45 ×104A,该电解槽的电解效率为 。
(1)氯化钠 氢氧化钠
(2)Ca2++ CO32-= CaCO3↓ ;Mg2+ + 2OH-= Mg(OH)2↓ 用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜。
(3)H2 阳极 2Cl-+2H2O Cl2↑+H2↑+2OH-(4)Na2SO3 + Cl2 + H2O = Na2SO4 + 2HCl
Cl2↑+H2↑+2OH-(4)Na2SO3 + Cl2 + H2O = Na2SO4 + 2HCl
(5)ηOH-=(W实 /W理)×100%=(113×32%×1.342×106)/(1.492×1.45×104×300×8)= 48.53/51.92 = 93.46%
解析试题分析:(1)由流程图可以看出:在该流程中可以循环的物质是氯化钠、氢氧化钠。(2)在一次精制中加入Na2CO3溶液发生反应:Ca2++ CO32-= CaCO3↓;加入NaOH发生反应:Mg2+ + 2OH-= Mg(OH)2↓。若食盐水不经过二次精制,用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜。(3)根据同种电荷相互排斥,异种电荷相互吸引的原则,Na+不断向F电极区移动,则E电极为阳极,发生的电极反应为:2Cl--2e-=Cl2↑ 。F电极为阴极。在阴极发生的反应为:2H++2e-=H2↑ 。则B处产生的气体是H2. 电解总反应的离子方程式为2Cl-+2H2O Cl2↑+H2↑+2OH- 。(4)氯气与Na2SO3发生氧化还原反应的化学方程式为:Na2SO3 + Cl2 + H2O = Na2SO4 + 2HCl。(5)m(NaOH实际)= 1.342吨/m3×113m3×32%=48.527t=4.8527×107g, m(NaOH理论)= 1.492×1.45×104×300×8g=5.19216×107g. 该电解槽的电解效率为m(NaOH实际)÷m(NaOH理论) ×100%=4.8527×107g÷5.19216×107g×100%=93.46%.
Cl2↑+H2↑+2OH- 。(4)氯气与Na2SO3发生氧化还原反应的化学方程式为:Na2SO3 + Cl2 + H2O = Na2SO4 + 2HCl。(5)m(NaOH实际)= 1.342吨/m3×113m3×32%=48.527t=4.8527×107g, m(NaOH理论)= 1.492×1.45×104×300×8g=5.19216×107g. 该电解槽的电解效率为m(NaOH实际)÷m(NaOH理论) ×100%=4.8527×107g÷5.19216×107g×100%=93.46%.
考点:考查在氯碱工业生产中的反应原理的化学方程式、离子方程式的书写、操作的原因及电解效率的计算的知识。

某原电池装置中盛有浓KOH溶液,若分别向__________(填“正”或“负”,下同)极通入可燃性气体,向__________极通入O2,则电路中就有电流通过,电流方向由__________极流向__________极,溶液中OH-向__________极移动。试完成下列问题:
| | 可燃性气体 | 正极反应 | 负极反应 | 电池总反应 | pH变化 |
| (1) | H2 | | | | |
| (2) | CO | | | | |
| (3) | CH4 | | | |
化学在能源开发与利用中起着十分关键的作用。氢气是一种新型的绿色能源,又是一种重要的化工原料。
Ⅰ.氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行如图所示的实验(图中所用电极均为惰性电极):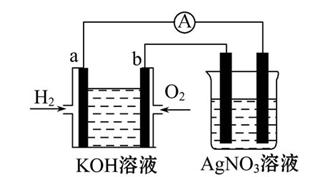
(1)对于氢氧燃料电池,下列表达不正确的是 。
| A.a电极是负极,OH-移向负极 |
| B.b电极的电极反应为:O2+2H2O+4e-=4OH- |
C.电池总反应式为:2H2+O2 2H2O 2H2O |
| D.电解质溶液的pH保持不变 |
(2)上图装置中盛有100 mL 0.1 mol·L-1 AgNO3溶液,当氢氧燃料电池中消耗氢气112 mL(标准状况下)时,此时图中装置中溶液的pH= (溶液体积变化忽略不计)。
Ⅱ.已知甲醇的燃烧热ΔH为-726.5 kJ·mol-1,在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为 ,正极的反应式为 。
理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为 (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) ΔH=-129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为______________________________________________________。
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如右图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________。
②100 ℃时反应Ⅰ的平衡常数为________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
| A.c(H2)减少 |
| B.正反应速率加快,逆反应速率减慢 |
| C.CH3OH 的物质的量增加 |
| D.重新平衡c(H2)/c(CH3OH)减小 |
(4)写出甲醇-空气-KOH溶液的燃料电池负极的电极反应式:__________________________________________________。

(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
①写出阳极电极反应式____________________________。
②写出除去甲醇的离子方程式__________________________________。
海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | S | HC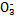 |
| 含量/(mg·L-1) | 9 360 | 83 | 200 | 1 100 | 16 000 | 1 200 | 118 |
(1)海水显弱碱性的原因是(用离子方程式表示): ,该海水中Ca2+的物质的量浓度为 mol·L-1。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过。
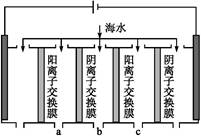
电渗析原理示意图
①阴极的电极反应为 。
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式: 。
③淡水的出口为a、b、c中的 出口。



 (1)工业上可利用反应Na(1)+ KCl(1) K(g)+ NaCl(1)来治炼金属钾,此反应利用了钠的还原性及___ _____,
(1)工业上可利用反应Na(1)+ KCl(1) K(g)+ NaCl(1)来治炼金属钾,此反应利用了钠的还原性及___ _____,