题目内容
【题目】氢气、氯气是中学实验室常见气体,在实验室可以利用该反应2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O,制备Cl2,并在实验室模拟工业制备盐酸,请回答下列问题:
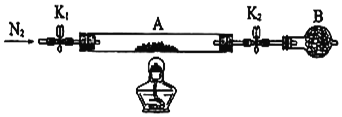
(1)甲组同学用下列装置制取H2和Cl2。
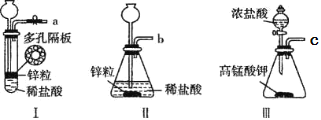
①实验室常用NaCl+H2SO4(浓)→NaHSO4+HCl↑反应制备HCl气体,该反应利用了浓硫酸的___性。
②用工业级锌粒(主要成分 Zn,含少量 FeS、Pb、Cu 等杂质)作原料,装置 I、Ⅱ均可以制取 H2,但装置 I 比装置Ⅱ更好,理由__________________________;检验氯气所用的试纸是_______________。
(2)乙组同学拟用甲组的装置 I、Ⅲ及下列装置(可以重复选用)模拟工业上制取盐酸。
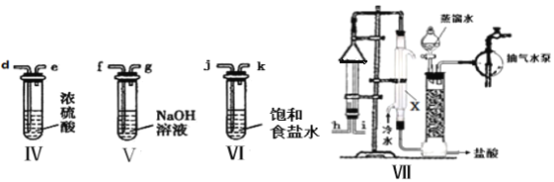
①乙组中氢气的部分实验装置连接是a-f-g-d……,其中装置Ⅴ的作用是_______,制取氯气并模拟合成盐酸的实验装置的合理连接顺序(用玻璃接口表示)为 c-__________。
②装置VII中仪器 X 的名称是_________ ,合成 HCl时需控制H2的体积略大于Cl2的体积,其目的是 ________;装置VII末端接抽气水泵的目的是___________。
(3)设计实验证明HCl极易溶于水且水溶液呈酸性:_____________________。
【答案】难挥发性(高沸点性) 装置Ⅰ可以实现即开即用,即关即停 淀粉-KI试纸 除氢气中的HCl及H2S等其他杂质气体 c—j—k—d—e—i 冷凝管 使氯气完全反应,防止氯气混入盐酸中 形成负压,使产生的HCl被水充分吸收 用滴有石蕊的水进行HCl的喷泉实验,形成红色喷泉,既证明HCl极易溶于水且水溶液呈酸性
【解析】
(1)I、II、III装置为常见的固液制气装置,其中I为启普发生器原理,可以通过控制止水夹让反应即开即用,即关即停。(2)利用甲组的III装置制取Cl2,再利用乙组可选用的装置除去Cl2中的杂质;利用甲组的I装置制取H2,再利用乙组可选用的装置除去H2中的杂质,将得到的纯净的Cl2和H2通入VII装置,为使其充分混合并反应,密度小的H2从h通入,密度大的Cl2从i通入,在VII装置中生成盐酸。(3) 证明HCl极易溶于水可利用喷泉实验,证明其水溶液呈酸性可用酸碱指示剂。
(1)①NaCl+H2SO4(浓)=NaHSO4+HCl↑,该反应的原理是难挥发性酸制取挥发性酸。
②装置 I为启普发生器原理,可以通过控制止水夹让反应即开即用,即关即停;氯气具有强氧化性,检验氯气所用的试纸是湿润的淀粉-KI试纸,现象是变蓝然后褪色。
(2)①由上述分析可知,利用甲组的III装置制取Cl2,再利用乙组可选用的装置除去Cl2中的杂质,先用饱和食盐水除去HCl,再用浓硫酸除去水蒸气,利用甲组的I装置制取H2,再利用V装置的氢氧化钠除去H2中的HCl及H2S等杂质,之后将得到的纯净的Cl2和H2通入VII装置,为使其充分混合并反应,密度小的H2从h通入,密度大的Cl2从i通入,在VII装置中生成盐酸。所以制取氯气并模拟合成盐酸的实验装置的合理连接顺序为c—j—k—d—e—i。
②由图可知,X为冷凝管;合成 HCl时需控制H2的体积略大于Cl2的体积,是为了使氯气完全反应,防止氯气混入盐酸中;抽气水泵可以形成负压,使产生的HCl被水充分吸收。
(3) 证明HCl极易溶于水可利用喷泉实验,证明其水溶液呈酸性可用酸碱指示剂,即用滴有石蕊的水进行HCl的喷泉实验,形成红色喷泉,既证明HCl极易溶于水且水溶液呈酸性。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案