题目内容
【题目】如图是一块非常独特的手表,用 H~Mg 12 种元素分别表示 1:00~12:00,关于此表的下列说法中不正确的是( )
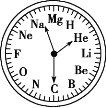
A.2:00 时的时针和 12:00 时的分针所指元素极难形成化合物
B.7:00 时,时针和分针所指元素可能形成相对分子质量为 100 的化合物
C.8:00 时,时针和分针所指元素形成的化合物属于碱性氧化物
D.3:00 时,时针所指元素的金属性比 11:00 时时针所指元素的金属性强
【答案】D
【解析】
A.He为惰性气体元素,与Mg极难形成化合物,故A正确;
B.N、Mg能形成相对分子质量为 100 的化合物Mg3N2,故B正确;
C.O、Mg能形成的化合物MgO,属于碱性氧化物,故C正确;
D.根据元素周期律,Li的金属性比Na的金属性弱,故D错误;
综上所述,答案为D。

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】用1.500mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示:
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 25.00 | 24.41 |
2 | 25.00 | 24.39 |
3 | 25.00 | 25.90 |
回答下列问题:
(1)量取待测液时,使用25.00ml移液管或______滴定管;
(2)实验中,需要润洗的仪器是:____________________;
(3)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是_____________________;
(4)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果__________(填“偏高”“偏低”“不变”,下同);若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果____________。
(5)未知浓度的NaOH溶液的物质的量浓度为__________ mol/L(保留小数点后3位有效数字)。