题目内容
【题目】SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:
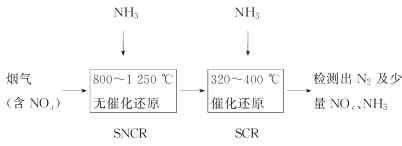
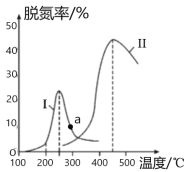
该方法中主要反应的热化学方程式为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ΔH=-1646 kJ/mol,如图所示,反应温度会直接影响SNCR技术的脱硝效率。
4N2(g)+6H2O(g) ΔH=-1646 kJ/mol,如图所示,反应温度会直接影响SNCR技术的脱硝效率。
回答下列问题:
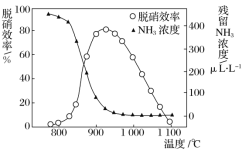
(1)SNCR技术脱硝的最佳温度选择925℃的理由是_______________________。
(2)SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是________________;
但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是___________。
【答案】925℃时脱硝效率高,残留氨浓度较小 没有使用催化剂,反应的活化能较大 因为脱硝主要反应是放热反应,温度过高,使脱硝主要反应的平衡逆向移动(或生成的N2与O2反应生成NO等其他合理答案)
【解析】
(1)根据图像,在925℃时脱销效率高,残留氨的浓度较小;
(2)根据流程,SNCR没有使用催化剂,SCR使用催化剂,使用催化剂降低活化能,加快反应,因此SNCR技术的反应温度较高;脱硝主要反应是放热反应,温度过高,使脱硝主要反应的平衡逆向移动,或者在较高温度下,N2与O2发生反应生成NO。

【题目】按要求回答下列问题:
(1)在200℃、101kPa时,0.5molH2(g)与足量I2(g)完全反应放出7.45kJ的热量,该反应的热化学方程式表示为____。
(2)根据键能数据估算
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
CH4(g)+4F2(g) =CF4(g)+4HF(g)的反应热ΔH为______kJ/mol
(3) 已知:①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH1=-a kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-b kJ/mol
③2H2(g) + O2(g) = 2H2O(g) ΔH3 = -c kJ/mol
a、b、c均大于0 则:反应①中,ΔS______(选填“>”、“<”或“=”)0;
2C(s)+4H2(g)+O2(g) = 2CH3OH(l) ΔH=_______kJ/mol。