题目内容
1.有关Na2CO3和NaHCO3的性质,下列叙述中错误的是( )| A. | 相同温度下,等浓度的Na2CO3和NaHCO3溶液的碱性比较,前者更强 | |
| B. | 常温时水溶性:Na2CO3>NaHCO3 | |
| C. | 在酒精灯加热的条件下,前者不分解,后者分解 | |
| D. | 将澄清的石灰水分别加入Na2CO3和NaHCO3溶液中,前者产生沉淀,后者不产生沉淀 |
分析 A.碳酸根离子水解能力强于碳酸氢根离子;
B.Na2CO3比NaHCO3易溶于水;
C.NaHCO3不稳定,加热易分解;
D.Na2CO3和NaHCO3都能与澄清的石灰水反应生成沉淀.
解答 解:A.碳酸根离子水解能力强于碳酸氢根离子,所以相同温度下,等浓度的Na2CO3和NaHCO3溶液的碱性比较,前者更强,故A正确;
B.常温时水溶性:Na2CO3>NaHCO3,故B正确;
C.NaHCO3不稳定,加热易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,碳酸钠受热不易分解,较稳定,故C正确;
D.Na2CO3和NaHCO3都能与澄清的石灰水反应生成沉淀,故D错误;
故选:D.
点评 本题考查Na2CO3和NaHCO3性质的异同,把握Na2CO3和NaHCO3性质是解题关键,题目难度不大.

练习册系列答案
相关题目
12.已知短周期元素A和B的离子A2+和B2-具有相同的电子层结构,则下列叙述正确的是( )
| A. | A2+的半径比B2-的半径小 | B. | A的原子序数比B小 | ||
| C. | A和B原子的电子层数相等 | D. | A和B原子的最外层电子数相等 |
9.下列描述与所得结论正确的是( )
| 选项 | 描述 | 结论 |
| A | 化合物A在熔融状态下可以导电 | A为离子化合物 |
| B | 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有Na+,无K+ |
| C | 将a、c两种金属相连后投到稀硫酸溶液中,a表面产生气泡 | 金属性a>c |
| D | NH4NO3溶液和稀HNO3溶液都可以使石蕊变红 | 它们均能电离出H+ |
| A. | A | B. | B | C. | C | D. | D |
16.X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增.X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.下列说法正确的是( )
| A. | 室温下,0.1 mol/LW的气态氢化物的水溶液的pH>1 | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | Y单质在一定条件下可以与氧化铁发生置换反应 | |
| D. | 原子半径由小到大的顺序:X<Y<Z<W |
6.生产、生活中离不开各类化学物质,下列化学物质属于盐类的是( )
| A. | 生石灰 | B. | 钻石 | C. | 水晶 | D. | 苏打 |
13.下列有机物的结构简式表示正确的是( )
| A. | 乙酸乙酯:CH3COOCH3CH2 | B. | 硝基苯: | ||
| C. | 丙烯:CH2CHCH3 | D. | 二甲醚:CH3OCH3 |
10.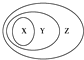 下表的一些物质或概念间的从属关系中不符合图示要求的是( )
下表的一些物质或概念间的从属关系中不符合图示要求的是( )
 下表的一些物质或概念间的从属关系中不符合图示要求的是( )
下表的一些物质或概念间的从属关系中不符合图示要求的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 离子化合物 | 化合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A. | A | B. | B | C. | C | D. | D |
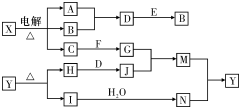 下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去).已知A、B为气态单质,F是地壳中含量最多的金属元素的单质,E、H、I为氧化物,E为黑色固体,I为红棕色气体,M为红褐色沉淀.
下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去).已知A、B为气态单质,F是地壳中含量最多的金属元素的单质,E、H、I为氧化物,E为黑色固体,I为红棕色气体,M为红褐色沉淀.