题目内容
9.Ⅰ化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题: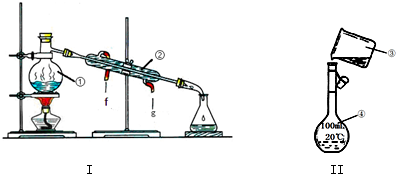
(1)写出上述图中仪器的名称:①蒸馏烧瓶;②冷凝管;
(2)若利用装置I分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有温度计,将仪器补充完整后进行的实验操作的名称为蒸馏;实验时仪器②中冷却水的进口为g(选填“f”或“g”).
(3)现需配制250mL 0.2mol•L-1 NaCl溶液,装置II是某同学转移溶液的示意图,图中有两处错误分别是未用玻璃棒引流,未采用250mL容量瓶.
Ⅱ已知 2Na2O2+2CO2=2Na2CO3+O2,因此Na2O2可在呼吸面具和潜水艇里作供氧剂.
(4)请用双线桥法标出上述方程式的电子转移方向和数目.2Na2O2+2CO2=2Na2CO3+O2
(5)若转移3mol电子,则所产生的氧气在标准状况下的体积为33.6L.
分析 (1)根据仪器的形状可确定仪器的名称和用途;
(2)分液沸点不同的液体混合物,可用蒸馏的方法,蒸馏时,应用温度计控制加热的温度,冷凝时,冷水应从下端进,上端出;
(3)应用25omL容量瓶,且用玻璃棒引流;
(4)(5)Na2O2中O元素化合价为-1价,在反应2Na2O2+2CO2=2Na2CO3+O2中,只有O元素化合价发生变化,O元素化合价分别由-1价降低到-2价、升高到0价,反应中Na2O2既是氧化剂又是还原剂,O2为氧化产物,Na2CO3为还原产物,该反应中转移2e-,以此解答;
解答 解:(1)由仪器的形状可知①为蒸馏烧瓶,②为冷凝管;
故答案为:蒸馏烧瓶;冷凝管;
(2)分液沸点不同的液体混合物,可用蒸馏的方法,蒸馏时,应用温度计控制加热的温度,且温度计应位于蒸馏烧瓶的支管口附近,冷凝时,冷水应从下端进,上端出,
故答案为:温度计;蒸馏;g;
(3)配制250mL 0.2mol•L-1NaCl溶液,应用250mL容量瓶,不能用100mL的容量瓶,转移液体必须用玻璃棒引流,以免液体溅出,
故答案为:未用玻璃棒引流;未采用250 mL容量瓶;
(4)在2Na2O2+2CO2═2Na2CO3+O2反应中,只有Na2O2中O元素的化合价发生变化,分别由-1价变化为0价和-2价,用双线桥法可表示为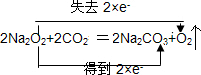 ;
;
故答案为: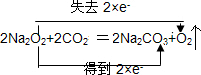 ;
;
(5)由2Na2O2+2CO2═2Na2CO3 +O2↑可知,转移2mol电子生成氧气为1mol,若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L;
故答案为:33.6L.
点评 本题考查常见仪器的使用、化学基本操作的方法以及氧化还原反应,题目难度不大,注意在学习中加强基础知识的积累本题考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.用已准确称量过的氯化钠固体配制1.00mol•L-1的NaCl溶液0.5L,需要用的仪器是( )
①坩埚 ②分液漏斗 ③容量瓶 ④烧杯 ⑤胶头滴管 ⑥烧瓶 ⑦玻璃棒 ⑧托盘天平 ⑨药匙.
①坩埚 ②分液漏斗 ③容量瓶 ④烧杯 ⑤胶头滴管 ⑥烧瓶 ⑦玻璃棒 ⑧托盘天平 ⑨药匙.
| A. | ③④⑤⑦⑨ | B. | ①②⑤⑥⑧ | C. | ③④⑤⑦ | D. | ③④⑤⑥ |
19.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是700 mL | |
| B. | 该合金中铜与镁的物质的量之比是2:1 | |
| C. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
 天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氢氧化钠溶液洗涤除去.
天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氢氧化钠溶液洗涤除去. ;羰基硫分子的电子式为
;羰基硫分子的电子式为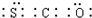 .
.