题目内容
4.已知:A、B、C、D四种元素的质子数都小于18,它们的核电荷数A<B<C<D;A与B可生成常见气体化合物AB2,每个AB2分子中含有22个电子;C元素原子的次外层电子数为最外层电子数的2倍,D元素原子的最外层电子数比次外层少1个,则各元素符号分别为:AC; BO; CSi; DCl.
分析 A、B、C、D四种元素的质子数都小于18,它们的核电荷数A<B<C<D;A与B可生成常见气体化合物AB2,每个AB2分子中含有22个电子,则A为碳元素、B为O元素;C元素原子的次外层电子数为最外层电子数的2倍,原子序数大于氧,只能处于第三周期,最外层电子数为4,故C为Si,D的原子序数大于Si,D元素原子的最外层电子数比次外层少1个,最外层电子数为7,故D为Cl.
解答 解:A、B、C、D四种元素的质子数都小于18,它们的核电荷数A<B<C<D;A与B可生成常见气体化合物AB2,每个AB2分子中含有22个电子,则A为碳元素、B为O元素;C元素原子的次外层电子数为最外层电子数的2倍,原子序数大于氧,只能处于第三周期,最外层电子数为4,故C为Si,D的原子序数大于Si,D元素原子的最外层电子数比次外层少1个,最外层电子数为7,故D为Cl,
故答案为:C;O;Si;Cl.
点评 本题考查元素推断,注意为短周期元素,关键是对核外电子排布规律的理解,比较基础.

练习册系列答案
相关题目
14.有①直馏汽油、②裂化汽油、③苯、④聚乙烯、⑤裂解气、⑥环己烷、⑦邻二甲苯、⑧环己烯(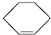 )其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是( )
)其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是( )
 )其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是( )
)其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是( )| A. | ②④⑤⑧ | B. | ②⑤⑧ | C. | ②④⑤⑦ | D. | ②④⑤⑦⑧ |
15.在容积不变的密闭容器中存在如下反应:2A(g)+B(g)?3C(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )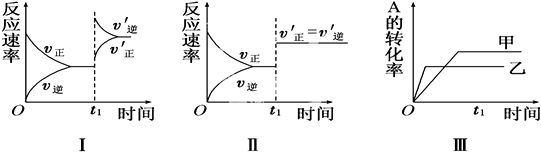

| A. | 图Ⅰ表示的是t1时刻升高温度对反应速率的影响 | |
| B. | 图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 | |
| D. | 图Ⅲ表示的是温度对平衡的影响,且乙的温度比甲高 |
16.某烃分子中有一个由C-C键构成的六元环,有一个C=C键,还有一个C≡C键,则能满足上述烃的分子式可能是( )
| A. | C8H10 | B. | C10H16 | C. | C12H22 | D. | C14H22 |
13.已知:2Cu(IO3)2+24KI+□ ═2CuI↓+13I2+□K2SO4+□
═2CuI↓+13I2+□K2SO4+□ ,生成的I2刚好消耗n mol S2O32-(S2O32-被氧化为S4O62-),则参加反应的Cu(IO3)2物质的量为( )
,生成的I2刚好消耗n mol S2O32-(S2O32-被氧化为S4O62-),则参加反应的Cu(IO3)2物质的量为( )
 ═2CuI↓+13I2+□K2SO4+□
═2CuI↓+13I2+□K2SO4+□ ,生成的I2刚好消耗n mol S2O32-(S2O32-被氧化为S4O62-),则参加反应的Cu(IO3)2物质的量为( )
,生成的I2刚好消耗n mol S2O32-(S2O32-被氧化为S4O62-),则参加反应的Cu(IO3)2物质的量为( )| A. | $\frac{n}{10}$ mol | B. | $\frac{n}{11}$ mol | C. | $\frac{n}{12}$ mol | D. | $\frac{n}{13}$ mol |
14.分类是科学研究的重要方法,下列物质分类不正确的是( )
| A. | 化合物:干冰,冰水混合物,烧碱,小苏打 | |
| B. | 非电解质:乙醇,四氯化碳,氯气,葡萄糖 | |
| C. | 同素异形体:活性炭,C60,C80,金刚石 | |
| D. | 混合物:漂白粉,纯净矿泉水,分析纯盐酸,石灰石 |