题目内容
4.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 12g金刚石晶体中含有的C-C的数目为2NA | |
| B. | 1L 1 mol•L-1AlCl3溶液中含有的Al3+数目为NA | |
| C. | 在标况下,11.2L氯气通入足量的NaOH溶液中转移电子数为NA | |
| D. | 18g重水(D2O)含有的中子数为10 NA |
分析 A、求出金刚石的物质的量,然后根据1mol金刚石中含2molC-C键来分析;
B、Al3+是弱碱阳离子,在溶液中会水解;
C、氯气与碱的反应为歧化反应;
D、重水的摩尔质量为20g/mol.
解答 解:A、12g金刚石的物质的量为1mol,而1mol金刚石中含2molC-C键,故A正确;
B、Al3+是弱碱阳离子,在溶液中会水解,故溶液中Al3+的个数小于NA,故B错误;
C、标况下,11.2L氯气的物质的量为0.5mol,氯气与碱的反应为歧化反应,1mol氯气转移1mol电子,故0.5mol氯气转移0.5mol电子,故C错误;
D、重水的摩尔质量为20g/mol,故18g重水的物质的量为0.9mol,而1mol重水中含10mol中子,故0.9mol重水中含9mol中子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
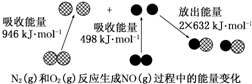
14.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
下列说法正确的是( )

下列说法正确的是( )
| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和O2(g)混合能直接生成NO(g) | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
15.X、Y、Z、W是原子序数依次增大的四种短周期元素.其中只有一种是金属元素,X、W同主族且能形成一种离子化合物WX;Y的气态氢化物、最高价氧化物的水化物可反应生成一种盐;Z原子的最外层电子数与其电子总数之比为3:4.下列说法中正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | 氢化物稳定性:Y>Z | |
| C. | WY3中只有离子键没有共价键 | |
| D. | X与Z可形成l0电子分子和18电子分子 |
12.已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O72-(橙色)+H2O?2H++2CrO42-(黄色)
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O72->Fe3+ | |
| C. | CrO42-和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
19.有一种基于乙醇酸性燃料电池原理设计的酒精检测仪,其原理是通过将乙醇氧化为乙酸来测定血液中乙醇的含量.下列有关说法正确的是( )
| A. | 电池工作时消耗5.6LO2,转移电子为1mol | |
| B. | 检测时,电解质溶液中的H+向负极移动 | |
| C. | 正极上发生的反应为:O2+4e-+2H2O=4OH- | |
| D. | 负极上发生的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
9.下列说法正确的是( )
| A. | 油脂的氢化是指将不饱和程度较高、熔点较低的液态油,通过催化加氢,可提高饱和度,转化成半固态的脂肪的过程 | |
| B. | 在酸性条件下,蔗糖水解成葡萄糖和果糖,它们都能被溴水氧化 | |
| C. | 氨基酸是两性化合物,只有两个不同氨基酸分子间脱水才能形成肽键 | |
| D. | 蛋白质遇到醋酸铅变性沉淀,加入大量的水,沉淀还可溶解 |
16.用下列实验装置进行相应的实验,不能达到实验目的是( )
| A | B | C | D | |
| 装置 | 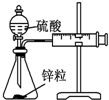 | 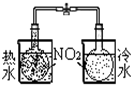 | 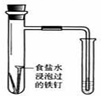 | 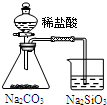 |
| 实验 | 结合秒表定量比较锌与不同浓度的稀硫酸反应的快慢 | 证明温度对化学平衡的影响 | 验证铁钉发生吸氧腐蚀 | 可证明非金属性Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
13.化学与科学、技术、社会、环境密切相关,下列有关说法正确的是( )
| A. | 节日燃放焰火,其颜色是某些金属元素焰色反应所致 | |
| B. | 糖类、蛋白质、油脂等营养物质都属于天然高分子化合物 | |
| C. | “温室效应”、“酸雨”、“光合作用”等现象都与CO2有关 | |
| D. | 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 |