题目内容
9.下列说法正确的是( )| A. | 油脂的氢化是指将不饱和程度较高、熔点较低的液态油,通过催化加氢,可提高饱和度,转化成半固态的脂肪的过程 | |
| B. | 在酸性条件下,蔗糖水解成葡萄糖和果糖,它们都能被溴水氧化 | |
| C. | 氨基酸是两性化合物,只有两个不同氨基酸分子间脱水才能形成肽键 | |
| D. | 蛋白质遇到醋酸铅变性沉淀,加入大量的水,沉淀还可溶解 |
分析 A.液态油与氢气发生加成反应生成固体脂肪的过程为油脂的氢化;
B.果糖分子中不含醛基,不会被溴水氧化;
C.相同的两个氨基酸分子也可以形成肽键;
D.蛋白质的变性为非可逆的,加水后不再溶解.
解答 解:A.液体油中含有不饱和键,将不饱和程度较高、熔点较低的液态油,通过催化加氢,可提高饱和度,转化成半固态的脂肪的过程称为油脂的氢化,故A正确;
B.在酸性条件下,蔗糖水解成葡萄糖和果糖,葡萄糖分子中含有醛基,能够被溴水氧化,而果糖分子中不含羟基,不会被溴水氧化,故B错误;
C.氨基酸分子中含有羧基和氨基,为两性化合物,两个氨基酸分子间经过脱水就可以形成肽键,可以是相同的氨基酸,也可以是不同的氨基酸,故C错误;
D.蛋白质遇到醋酸铅变性沉淀,该反应过程不可逆的,加入大量的水,沉淀不会溶解,故D错误;
故选A.
点评 本题考查了蛋白质的性质、油脂的组成及性质,题目难度不大,注意掌握蛋白质、油脂的组成及性质,明确蛋白质的变性与盐析的区别,为易错点.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
19.国家对食品、空气、药品安全问题越来越重视,下列说法中一定正确的是( )
| A. | 欧洲和北美洲的一些大城市上空二氧化氮浓度很高,其原因是这些地区硝酸工业发达 | |
| B. | 大气污染物中的二氧化硫能引起呼吸道疾病 | |
| C. | 天然的药物无任何毒副作用,可长期服用 | |
| D. | 长期食用二氧化硫含量超标的食品会破坏维生素B1,可通过服入碱性物质(如NaOH)的方法来消除二氧化硫中毒 |
17.心酮胺是治疗冠心病的药物,其结构简式如下图,下列描述中正确的是( )
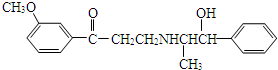
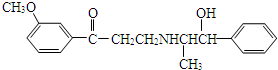
| A. | 该分子中含有酚羟基 | |
| B. | 该物质可以和浓氢溴酸发生取代反应 | |
| C. | 该物质可以和银氨溶液发生银镜反应 | |
| D. | 该分子苯环上的一氯取代物有6种 |
4.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 12g金刚石晶体中含有的C-C的数目为2NA | |
| B. | 1L 1 mol•L-1AlCl3溶液中含有的Al3+数目为NA | |
| C. | 在标况下,11.2L氯气通入足量的NaOH溶液中转移电子数为NA | |
| D. | 18g重水(D2O)含有的中子数为10 NA |
14.下列实验操作能达到预期实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验Fe2(SO4)3溶液中是否含有FeSO4 | 取少量溶液于试管,加入几滴0.1mol/L KMnO4溶液 |
| B | 证明Al(OH)3是两性氢氧化物 | 取Al(OH)3于试管A、B,分别滴加氨水与盐酸 |
| C | 使蛋白质能变性 | 向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,产生沉淀 |
| D | 除去Na2CO3中的NaCl | 溶解,加入AgNO3溶液至不再产生沉淀,静置,过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.下列离子方程式正确的是( )
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32- | |
| B. | 向硫酸氢钠溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| C. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 | |
| D. | 硫氢根离子的电离方程式:HS-+H2O?H3O++S2- |
18.NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 78gNa2O2与62gNa2O中所含阴离子数目都是NA | |
| B. | 常温常压下,NA个Cl2通入水中,转移电子数为NA | |
| C. | 电解精炼铜时,若阴极得到2NA个电子,则阳极质量减少64g | |
| D. | 5.6g铁粉与足量硫粉充分反应,转移电子数为0.3NA |
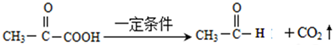

 .
.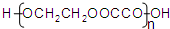 .
.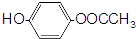 .
.