题目内容
下列反应中亚硫酸溶液表现的性质与另外三种不同的是( )
| A、能使酸性高锰酸钾溶液褪色 |
| B、在空气中久置,溶液pH变小 |
| C、能使溴水褪色 |
| D、加入氢氧化钡溶液产生白色沉淀 |
考点:含硫物质的性质及综合应用
专题:氧族元素
分析:亚硫酸具有较强的还原性,能被一些常见的氧化剂如溴水、酸性高锰酸钾、氧气、氯气等氧化;属于酸,具有酸的通性.
解答:
解:A、能使酸性高锰酸钾溶液褪色,是亚硫酸的还原性,故A不选;
B、在空气中久置,亚硫酸被氧化成硫酸,溶液pH变小,是亚硫酸的还原性,故B不选;
C、能使溴水褪色,是亚硫酸的还原性,故C不选;
D、加入氢氧化钡溶液产生白色沉淀,是发生了酸碱中和反应生成了难溶性的亚硫酸钡,故D选;
故选D.
B、在空气中久置,亚硫酸被氧化成硫酸,溶液pH变小,是亚硫酸的还原性,故B不选;
C、能使溴水褪色,是亚硫酸的还原性,故C不选;
D、加入氢氧化钡溶液产生白色沉淀,是发生了酸碱中和反应生成了难溶性的亚硫酸钡,故D选;
故选D.
点评:本题考查亚硫酸的性质,题目难度不大,本题注意还原性和酸性的判断角度,为解答该题的关键.

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列说法正确的是( )
| A、100mL 1 mol?L-1的CH3COOH溶液中含有CH3COOH分子0.1NA |
| B、等物质的量的N2和CO的质量均为28g |
| C、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| D、100mL 1mol/L的Na3PO4溶液中含有离子数多于0.4NA |
76.8g铜与适量浓硝酸反应,铜全部溶解,若NO3-减少2mol,则溶液中H+减少了( )
| A、2.2mol |
| B、3.2mol |
| C、4.4mol |
| D、4.8mol |
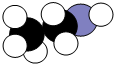 如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质说法不正确为( )
如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质说法不正确为( )| A、不能使紫色石蕊变红 |
| B、与碳酸钠反应 |
| C、能发生酯化反应 |
| D、能发生氧化反应催化剂 |
下列说法正确的是( )
| A、能与酸反应生成盐和水的氧化物一定是碱性氧化物 |
| B、把SO2通入溴水中,溴水立即褪色,这是由于SO2具有漂白作用 |
| C、将Ba(OH)2溶液滴到明矾溶液中,当SO42-恰好沉淀完全时,铝只以AlO2-形式存在 |
| D、在含有Cu(NO3)2、Mg(NO3)2、Fe(NO3)3溶液中加入过量锌粉,最先被还原的是Cu2+ |
将铝投入到一定量的NaOH溶液中,充分反应后,有2mol的电子发生了转移.则参加反应的铝的物质的量为( )
A、
| ||
| B、1mol | ||
| C、2mol | ||
D、
|
下列实验操作中需要用玻璃棒的是( )
①过滤 ②蒸发 ③溶解 ④蒸馏 ⑤萃取.
①过滤 ②蒸发 ③溶解 ④蒸馏 ⑤萃取.
| A、①②③ | B、②③④ |
| C、③④⑤ | D、①④⑤ |
下列实验操作或装置错误的是( )
A、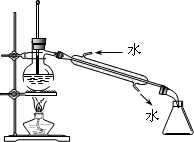 蒸馏 |
B、 过滤 |
C、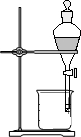 萃取 |
D、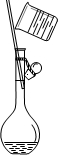 转移溶液 |