题目内容
将铝投入到一定量的NaOH溶液中,充分反应后,有2mol的电子发生了转移.则参加反应的铝的物质的量为( )
A、
| ||
| B、1mol | ||
| C、2mol | ||
D、
|
考点:铝的化学性质
专题:几种重要的金属及其化合物
分析:铝投入到一定量的NaOH溶液中,发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由反应可知,2molAl反应转移6mol电子,以此计算.
解答:
解:铝投入到一定量的NaOH溶液中,发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由反应可知,2molAl反应转移6mol电子,则有2mol电子发生转移,参加反应的Al为2mol×
=
mol,
故选D.
| 2 |
| 6 |
| 2 |
| 3 |
故选D.
点评:本题考查Al的性质及化学反应的计算,为基础性习题,把握发生的反应及Al与转移电子的关系为解答的关键,侧重分析能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、氧化钠与水反应:O2-+H2O=2OH- |
| B、NO2与水反应:3NO2+H2O=2H++2NO3-+NO |
| C、用食醋除水垢中的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- |
下面有关Na2CO3与NaHCO3的性质比较中错误的是( )
| A、相同浓度溶液的碱性:Na2CO3>NaHCO3 |
| B、同温下在水中的溶解度:Na2CO3>NaHCO3 |
| C、滴加同浓度的硫酸,反应先放出气泡的是Na2CO3 |
| D、热稳定性:NaHCO3<Na2CO3 |
下列有关有机物同分异构体说法中不正确的是( )
| A、分子式为C4H8的同分异构体共有(不考虑立体异构)5种 |
| B、立方烷(C8H8)的六氯取代物有3种 |
| C、分子式为C5H12O的同分异构体中属于醇类的有7种 |
D、 的一溴取代物有4种 的一溴取代物有4种 |
下列反应中亚硫酸溶液表现的性质与另外三种不同的是( )
| A、能使酸性高锰酸钾溶液褪色 |
| B、在空气中久置,溶液pH变小 |
| C、能使溴水褪色 |
| D、加入氢氧化钡溶液产生白色沉淀 |
下列有关化学反应速率的说法中,正确的是( )
| A、100mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C、二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| D、汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |
已知:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O,2FeCl2+Cl2=2FeCl3,下列物质的氧化性由强到弱的顺序是( )
| A、KMnO4>Cl2>FeCl3 |
| B、Cl2>KMnO4>FeCl3 |
| C、FeCl3>Cl2>KMnO4 |
| D、FeCl3>KMnO4>Cl2 |
下列装置或操作不能达到实验目的是( )
A、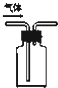 利用排空气法收集CO2 利用排空气法收集CO2 |
B、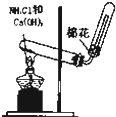 实验室制取NH3 实验室制取NH3 |
C、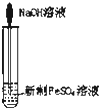 实验室制取Fe(OH)2 实验室制取Fe(OH)2 |
D、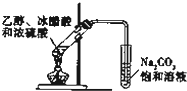 实验室制乙酸乙酯 实验室制乙酸乙酯 |
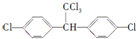 的有机物中,分子中最多有
的有机物中,分子中最多有