题目内容
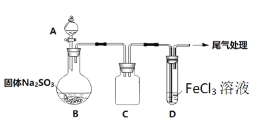
【题目】某校化学兴趣小组探究SO2与FeCl3溶液的反应,装置如下图所示。
已知:
i.Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。
ii.生成Fe(HSO3)2+离子的反应为:Fe3+ +HSO![]() Fe(HSO3)2+ 。
Fe(HSO3)2+ 。
步骤一:实验准备:
如上图连接装置,并配制100mL 1.0 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管D 中。
(1)配制100mL1.0 mol·L-1 FeCl3溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和______,装置C的作用为:________________。
(2)用离子方程式解释1.0 mol·L-1 FeCl3溶液(未用盐酸酸化)pH=1的原因:________
步骤二:预测实验
(3)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色。
该小组同学预测的理论依据为:________________
步骤三:动手实验
(4)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,将混合液放置12小时,溶液才变成浅绿色。
①SO2与FeCl3溶液反应生成了Fe(HSO3)2+离子的实验证据为:__________。证明浅绿色溶液中含有Fe2+的实验操作为:_____________ 。
②为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了如下实验。
实验I | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
实验II | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
综合上述实验探究过程,得出的结论为:____________。
步骤四:反思实验:
(5)在制备SO2的过程中,同学们发现,使用70%的硫酸比用98%的浓硫酸反应速率快,分析其中的原因是_________。
【答案】100mL容量瓶 安全瓶 防倒吸 Fe3++3H2OFe(OH)3+3H+ SO2有强还原性,FeCl3有强氧化性,发生氧化还原反应生成Fe2+或SO2+2 Fe3++2H2O=SO![]() +4H++2 Fe2+ 溶液变成红棕色 向反应后的溶液中加入铁氰化钾{K3[Fe(CN)6]}溶液 加热、提高FeCl3溶液的酸性会缩短浅绿色出现的时间 反应本质是H+与SO
+4H++2 Fe2+ 溶液变成红棕色 向反应后的溶液中加入铁氰化钾{K3[Fe(CN)6]}溶液 加热、提高FeCl3溶液的酸性会缩短浅绿色出现的时间 反应本质是H+与SO![]() 反应,70%的硫酸中含水较多,c(H+)和c(SO
反应,70%的硫酸中含水较多,c(H+)和c(SO![]() )都较大,生成SO2速率更快
)都较大,生成SO2速率更快
【解析】
探究SO2与FeCl3溶液的反应,根据图示,B中亚硫酸钠与硫酸反应放出二氧化硫,二氧化硫易溶于水,为了防止倒吸,需要安装安全瓶,将生成的二氧化硫通入FeCl3溶液中反应,通过观察现象进行实验。在解答时要结合题目所给信息和化学反应原理分析解答。
(1) 配制溶液的步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为天平、药匙、量筒、烧杯、100mL容量瓶、玻璃棒、胶头滴管,其中玻璃仪器有量筒、烧杯、100mL容量瓶、玻璃棒、胶头滴管,缺少的仪器:100mL容量瓶;装置C为安全瓶,防止D中溶液倒吸入B中,故答案为:100mL 容量瓶;安全瓶,防止倒吸;
(2) FeCl3为强酸弱碱盐,水解后溶液显酸性,Fe3++3H2OFe(OH)3+3H+,故答案为:Fe3++3H2OFe(OH)3+3H+;
(3) SO2具有还原性,能够与FeCl3溶液发生氧化还原反应生成亚铁离子,SO2+2 Fe3++2H2O=SO![]() +4H++2 Fe2+,因此反应的现象为溶液由棕黄色变成浅绿色,故答案为:SO2有强还原性,FeCl3有强氧化性,发生氧化还原反应生成Fe2+(或SO2+2 Fe3++2H2O=SO
+4H++2 Fe2+,因此反应的现象为溶液由棕黄色变成浅绿色,故答案为:SO2有强还原性,FeCl3有强氧化性,发生氧化还原反应生成Fe2+(或SO2+2 Fe3++2H2O=SO![]() +4H++2 Fe2+);
+4H++2 Fe2+);
(4)①Fe(HSO3)2+离子为红棕色,当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,说明反应生成了Fe(HSO3)2+离子;Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+,证明浅绿色溶液中含有Fe2+的实验操作为向反应后的溶液中加入铁氰化钾溶液{K3[Fe(CN)6]},生成蓝色沉淀,故答案为:溶液变成红棕色;向反应后的溶液中加入铁氰化钾{K3[Fe(CN)6]}溶液;
②根据实验I,将溶液微热3 min,溶液颜色变为浅绿色,根据实验II,向溶液中通入SO2气体,溶液立即变为红棕色,几分钟后,发现溶液颜色变成浅绿色,说明加热、提高FeCl3溶液的酸性会缩短浅绿色出现的时间,故答案为:加热、提高FeCl3溶液的酸性会缩短浅绿色出现的时间;
(5)亚硫酸钠与硫酸反应放出二氧化硫的本质是H+与SO![]() 反应,98%的浓硫酸中H2SO4电离的很少,而70%的硫酸中含水较多,H2SO4几乎完全电离,导致c(H+)和c(SO
反应,98%的浓硫酸中H2SO4电离的很少,而70%的硫酸中含水较多,H2SO4几乎完全电离,导致c(H+)和c(SO![]() )都较大,生成SO2速率更快,故答案为:反应本质是H+与SO
)都较大,生成SO2速率更快,故答案为:反应本质是H+与SO![]() 反应,70%的硫酸中含水较多,c(H+)和c(SO
反应,70%的硫酸中含水较多,c(H+)和c(SO![]() )都较大,生成SO2速率更快。
)都较大,生成SO2速率更快。

【题目】某学习小组为了探究CH3COOH的电离情况,进行了如下实验。
(实验一)测定醋酸溶液中CH3COOH的物质的量浓度。
用 0.2000mol/L 的 NaOH 溶液滴定 20.00mL 醋酸溶液,3 次滴定所消耗NaOH溶液的体积如下:
实验次数 | 1 | 2 | 3 |
消耗NaOH 溶液的体积/mL | 20.05 | 20.00 | 19.95 |
(1)量取 20.00 mL 醋酸溶液所用的仪器是_____(填字母)
|
|
|
|
a | b | c | d |
(2)以上醋酸溶液中CH3COOH的物质的量浓度为_____
(实验二)探究浓度对CH3COOH电离程度的影响。
用 pH 计测定 25℃时不同浓度的醋酸的 pH,结果如下:
浓度/(mol·L-1) | 0.2000 | 0.1000 | 0.0100 |
pH | 2.83 | 2.88 | 3.38 |
(3)根据表中数据可知CH3COOH是_____电解质(填“强”或“弱”) 得出此结论的依据是_____
(4)写出CH3COOH的电离方程式_____