题目内容
18.下列事实不能用有机物分子内基团间的相互作用解释的是( )| A. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使高锰酸钾酸性溶液褪色,甲烷和苯不能使高锰酸钾酸性溶液褪色 | |
| D. | 苯与硝酸在50~60°C发生取代反应,甲苯与硝酸在30°C就能发生取代反应 |
分析 A、苯环对酚羟基影响的结果是酚羟基具有酸性;
B、从苯环对侧链影响的角度分析;
C、根据C=C官能团的性质分析;
D、甲基对苯环有影响.
解答 解:A、在苯酚中,由于苯环对-OH的影响,酚羟基具有酸性,对比乙醇,虽含有-OH,但不具有酸性,能说明上述观点,故A不选;
B、乙烯和乙烷结构不同,乙烯含有C=C,可发生加成反应,不能用上述观点证明,故B选;
C、甲苯和甲烷中都含有-CH3,但二者性质不同,说明苯环对侧链影响,故C不选;
D、甲苯和苯中都含有苯环,二者性质不同,可说明侧链对苯环有影响,故D不选.
故选B.
点评 本题考查有机物的结构和性质,题目难度不大,注意有机物的原子团之间相互影响的特点.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
8.2010年诺贝尔化学奖化学授予理查德•赫克等三位科学家,以表彰他们在“钯催化交叉偶联”方面的研究.下面关于催化剂的说法正确的是( )
| A. | 催化剂能够改变反应的反应热 | |
| B. | 催化剂能够改变反应物的活化分子百分数 | |
| C. | 催化剂能改变反应物的转化率 | |
| D. | 催化剂通过升高反应的活化能来加快反应速率 |
9.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 四种元素位于同一周期 | B. | b+1=d-1 | ||
| C. | 氢化物稳定性:H2Y>HZ | D. | 离子的氧化性:W3+>X+ |
6.具有下列电子层结构的原子,其对应的元素一定属于同一周期的是( )
| A. | 两种元素原子的电子层上全部都是s电子 | |
| B. | 最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子 | |
| C. | 3p能级上只有1个空轨道的原子和3p能级上只有1个未成对电子的原子 | |
| D. | M层上的s、p能级上都填满了电子而d轨道未排电子的两种原子 |
13.在乙醇发生的各种反应中,断键方式不正确的是( )
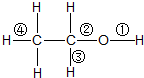

| A. | 与金属钠反应时,键①断裂 | |
| B. | 与HCl反应生成氯乙烷时,键②断裂 | |
| C. | 与醋酸、浓硫酸共热时,键②断裂 | |
| D. | 与浓硫酸共热至170℃时,键②和④断裂 |
3.下列实验操作可以达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 检验工业废水中是否含有苯酚 | 在试管中加入2 mL工业废水样品,然后加入2滴浓溴水,振荡,观察是否产生白色沉淀 |
| B | 验证乙醛中含有醛基 | 在试管中加入2 mL10%的CuSO4溶液,然后加入4至6滴2%的NaOH溶液振荡,再加入0.5 mL乙醛溶液加热煮沸,观察是否出现红色沉淀 |
| C | 提纯粗苯甲酸 | 将1g粗苯甲酸溶于50mL蒸馏水,加热使之全部溶解,趁热过滤,将滤液冷却结晶,滤出晶体 |
| D | 证明溴乙烷发生消去反应生成乙烯 | 将产生的气体通入酸性高锰酸钾溶液中,观察溶液是否褪色 |
| A. | A | B. | B | C. | C | D. | D |
10.现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍.下列说法正确的是( )
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 气态氢化物的稳定性:Z>M | |
| C. | 简单离子半径由大到小的顺序是:Z>M>Y | |
| D. | X2Z与X2M比较,稳定性:X2Z>X2M |
7.对现代元素周期表的提出做出最重要贡献的科学家是( )
| A. | 门捷列夫(俄国) | B. | 纽兰兹(英国) | C. | 迈耶尔(德国) | D. | 拉瓦锡(法国) |
8.室温下,同种规格的铝片分别与下列物质混合,产生氢气速率最大的是( )
| A. | 0.1 mol/L的盐酸15mL | B. | 0.15 mol/L 的硫酸溶液8mL | ||
| C. | 0.2 mol/L 的盐酸12mL | D. | 18 mol/L的浓硫酸15mL |