题目内容
8.在容积一定的密闭容器中,反应2A?B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是( )| A. | 正反应是吸热反应,且A是气态 | |
| B. | 正反应是放热反应,且A不是气态 | |
| C. | 其他条件不变,加入少量A,该平衡不移动 | |
| D. | 改变压强对该平衡的移动无影响 |
分析 根据外界条件(浓度、温度、压强)对化学平衡的影响,可以根据平衡移动原理,利用公式ρ=$\frac{m}{V}$,根据容器内气体的密度增大,来判断容器内气体的密度是否增大进行分析.
解答 解:A、因温度升高,平衡向吸热的方向移动,若正反应是吸热反应,平衡正向移动,如果A为气态时,根据ρ=$\frac{m}{V}$,m不变,V不变,所以密度不会改变,与题意矛盾,所以A不是气体,故A错误;
B、根据ρ=$\frac{m}{V}$,在体积不变情况下,容器内气体的密度增大,所以一定是质量增大,A一定不是气体,且升高温度平衡向右进行,即正反应方向是吸热方向,故B错误;
C、根据题意可知A是固体,A的量的增减不会引起化学平衡的移动,故C正确;
D、该反应是一个化学反应前后气体物质的量变化的反应,所以改变压强对该平衡的移动有影响,故D错误.
故选C.
点评 本题考查化学平衡,解答本题的关键是熟悉外界条件(浓度、温度、压强)对化学平衡的影响,注意条件的适用范围,然后再根据化学平衡移动原理来对问题做出正确的判断即可,难度不大.

练习册系列答案
相关题目
18.下列说法不正确的是( )
| A. | Na2O、Na2O2组成元素相同,均与H2O反应,均属于碱性氧化物 | |
| B. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈无色 | |
| C. | NO、SO2、NO2都是大气污染气体,在空气中都不能稳定存在 | |
| D. | SiO2是酸性氧化物,能与NaOH溶液反应 |
19.已知C(s)+CO2(g)?2CO(g)正反应方向是吸热过程,下列可使正反应速率增大的措施是( )
①减小容器体积使增大压强
②增加碳的量
③恒容时通入CO2
④恒压下充入N2
⑤恒容下充入N2
⑥降低温度.
①减小容器体积使增大压强
②增加碳的量
③恒容时通入CO2
④恒压下充入N2
⑤恒容下充入N2
⑥降低温度.
| A. | ①③⑤ | B. | ②④ | C. | ①③ | D. | ①③⑥ |
16.某甲烷燃料电池构造示意图如下,关于该电池的说法不正确的是( )
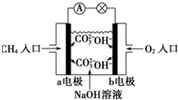

| A. | a极是负极,发生氧化反应 | |
| B. | 正极的电极反应是:O2+2H2O+4e-=4OH- | |
| C. | 该甲烷燃料电池的总反应:CH4+2O2=CO2+2H2O | |
| D. | 甲烷燃料电池是环保电池 |
3.下列有关金属腐蚀与防护的说法不正确的是( )
| A. | 钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-═4OH- | |
| B. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
13.氨分子空间构型是三角锥形,键角小于109°28′,而甲烷是正四面体,键角等于109°28′,键角差别是因为( )
| A. | 两种分子的中心原子杂化轨道类型不同,NH3为sp2杂化,而CH4是sp3杂化 | |
| B. | NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 | |
| C. | NH3分子中有一对未成键的孤电子对,它对成键电子对的排斥作用较强 | |
| D. | 氨气分子是极性分子而甲烷是非极性分子 |
17.下列变化中,不破坏化学键的是( )
| A. | HCl溶于水 | B. | 碘的升华 | C. | 水的电解 | D. | 金刚石熔化 |
10.下列各组物质中,互为同系物的是( )
| A. | 葡萄糖与蔗糖 | B. | CH2=CH-CH3和CH2=CH-CH2-CH3 | ||
| C. | 甲烷与丙烷 | D. | 丁烷与异丁烷 |
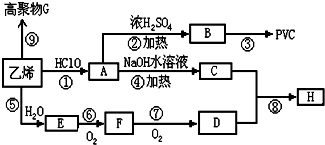
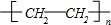 ;
;