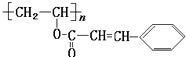题目内容
【题目】某校合作学习小组的同学设计实验验证钠在二氧化碳中燃烧的产物。回答下列问题:
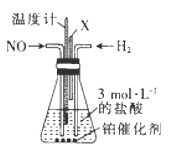
(1)甲组同学利用下列装罝制取干燥纯净的二氧化碳。仪器X的名称是 , 装置B中盛装的试剂是。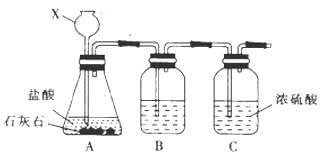
(2)乙组同学利用甲组制得的CO2并选用下列装置(可重复使用)验证钠在二氧化碳中燃烧的产物中是否含有CO。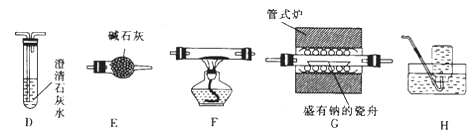
①F中盛装的试剂是。
②装置正确的连接顺序为C→→→→E→→H。
③证明燃烧的产物中含有CO的现象是。
(3)丙组同学取乙组同学在G装置中所得的固体于试管中,加入足量稀盐酸,有气体产生且试管底部有黑色不溶物,则固体产物中一定有(填化学式)。
【答案】
(1)长颈漏斗,饱和NaHCO3溶液
(2)CuO,G,E,D,F,D,F中黑色粉末变为红色(或装置F之前的D中澄淸石灰水不变浑浊,装置F之后的Ⅰ中澄淸石灰水变浑浊)
(3)Na2CO3和C
【解析】本题主要考查对于“验证钠在二氧化碳中燃烧的产物”探究实验的评价。
(1)仪器X的名称是长颈漏斗,装置B中盛装的试剂是用来除去氯化氢杂质的饱和NaHCO3溶液。
(2)①F中盛装的试剂是CuO。
②实验步骤中应先将钠在二氧化碳中燃烧的产物通过E除去剩余二氧化碳,通过D确认,再通过F使CO转化为CO2,通过D验证,所以装置正确的连接顺序为C→G→E→D→F→D→H。
③证明燃烧的产物中含有CO的现象是F中黑色粉末变为红色(或装置F之前的D中澄淸石灰水不变浑浊,装置F之后的Ⅰ中澄淸石灰水变浑浊)。
(3)该气体为二氧化碳,黑色不溶物为单质炭,则固体产物中一定有Na2CO3和C。
【考点精析】本题主要考查了钠的化学性质的相关知识点,需要掌握钠的化学性质:与非金属反应;与水反应;与酸反应;与盐溶液反应才能正确解答此题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】利用废碱渣(主要成分为Na2CO3)处理硫酸厂尾气中的SO2 , 可制得无水Na2SO3(成品),其流程如图所示。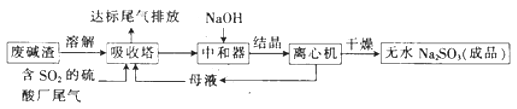
(1)某硫酸厂排放出的尾气中SO2的含量特别髙,而废碱渣的量不足,此时“吸收塔”内发生反应的离子方程式为(不考虑H2O与SO2反应)。
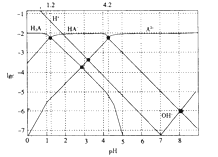
(2)亚硫酸钠的溶解度曲线如图所示,则上述流程中“结晶”的方法是(填“蒸发结晶”或“降温结晶”),图中a点所示分散系类别为(填“浊液”“胶体”或“溶液”)。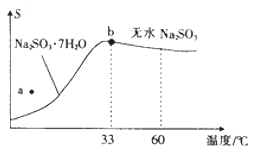
(3)仅用BaCl2、H2O2和过量稀盐酸的混合溶液难以检出“成品”中的SO32- , 原因是“成品”中含有某种杂质阴离子。
①该杂质阴离子为(填离子符号)。
②25℃时,部分钡盐的Ksp如下表所示。
化学式 | BaSO4 | BaSO3 |
Ksp | 1.1×10-10 | 5.5×10-7 |
将得到的“成品”溶于水,测得溶液中SO32-的浓度为0.5mol L-1 , 为杂质阴离子浓度的10倍,向该溶液中加入等体积、0.5mol·L-1的BaCl2溶液,充分反应后c(Ba2+)=mol L-1。(混合时溶液体积的变化忽略不计)
(4)某同学采用如下方法检验SO32-:![]()
①洗涤时使用的试剂最好为(填字母)。
a.稀HNO3 b.蒸馏水 c.稀H2SO4
②根据上述流程中的数据(w、x、y) (填“能”或“不能”)计算出成品试样中SO32-的百分含量,若能,则SO32-的百分含量为(若不能,则此空不填);若不能,则理由是(若能,则此空不填)。