题目内容
【题目】下列实验对相应的现象解释不正确的是
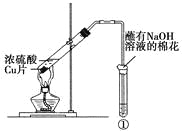
选项 | ①中试剂 | ①中现象 | 解释 |
A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
A.AB.BC.CD.D
【答案】A
【解析】
A.在加热的条件下,铜和浓硫酸反应生成SO2,SO2溶于水溶液显酸性,则溶液中NO3-能把SO2氧化生成硫酸,进而生成硫酸钡白色沉淀,A不正确;
B.SO2具有漂白性,能使品红溶液褪色,B正确;
C.SO2溶于水显酸性,能使紫色的石蕊试液显红色,C正确;
D.SO2具有还原性,酸性高锰酸钾溶液具有氧化,因此SO2能使酸性高锰酸钾溶液褪色,D正确;
答案选A。
【点晴】
(1)SO2性质的多面性:二氧化硫通入下列溶液中的现象与其体现的性质比较
溶液 | 石蕊试液 | 加有酚酞的 | 酸性KMnO4 | 溴水 | 品红溶液 | 氢硫酸 |
现象 | 变红 | 褪色 | 褪色 | 褪色 | 褪色 | 生成浅黄色沉淀 |
SO2的性质 | 溶于水显酸性 | 溶于水显酸性 | 还原性 | 还原性 | 漂白性 | 氧化性 |
(2)SO2的学习主要抓住三点:一是酸性氧化物,类似于CO2,如能使澄清石灰水变浑浊,BaSO3是沉淀等。二是其具有较强的还原性,易被氧化。三是漂白性。

练习册系列答案
相关题目