题目内容
【题目】新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是( )
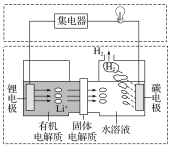
A.碳极发生的反应:2H2O+2e-=H2↑+2OH-
B.有机电解质和水溶液不可以互换区域
C.理论上外电路中每转移1 mol电子,负极消耗的质量为7 g
D.若该电池可以充电,充电时碳极接外加电源的负极,锂极接外加电源的正极
【答案】D
【解析】
锂能够与水反应,则形成原电池时,锂为负极,碳为正极,且负极不能与水接触,负极反应为Li-e-=Li+,正极反应为2H2O+2e-=H2↑+2OH-,结合原电池原理分析解答。
A.根据图示和上述分析,碳为正极,正极反应式为2H2O+2e-=H2↑+2OH-,故A正确;
B.金属Li可以和水发生反应生成氢氧化锂和氢气,但和有机电解质不反应,所以有机电解质和水溶液不可以互换区域,故B正确;
C.根据Li-e-=Li+可知,外电路中每转移1mol电子,消耗1moLi,质量为7g,故C正确;
D.充电时,锂电极发生还原反应生成Li,应连接电源负极,碳极接外加电源的正极,故D错误;
故选D。

练习册系列答案
相关题目
【题目】下列实验对相应的现象解释不正确的是
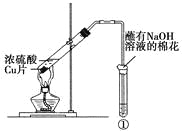
选项 | ①中试剂 | ①中现象 | 解释 |
A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
A.AB.BC.CD.D