题目内容
 某研究性学习小组设计了一组实验验证元素性质的递变性规律.
某研究性学习小组设计了一组实验验证元素性质的递变性规律.(1)甲同学想验证同周期元素金属性强弱的规律,最好选用第
三
三
周期的钠、镁、铝
钠、镁、铝
三种元素.最简单的实验是将大小相近的三小块金属分别投入相同浓度的稀盐酸中,观察现象.应该看到的现象是:①
钠剧烈反应,可能着火或爆炸
钠剧烈反应,可能着火或爆炸
,②
镁反应较剧烈,产生大量气泡
镁反应较剧烈,产生大量气泡
,③
铝反应比镁缓慢,有较多的气泡产生
铝反应比镁缓慢,有较多的气泡产生
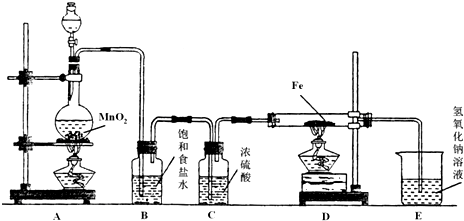
.(2)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强.他设计了如图所示装置以验证氮、碳、硅元素的非金属性强弱.
该同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成.
①写出所选用物质的化学式:
A:
HNO3
HNO3
;B:CaCO3
CaCO3
;C:Na2SiO3
Na2SiO3
.②写出烧杯中发生反应的离子方程式:
CO2+SiO32-+H2O═H2SiO3↓+CO32-或2CO2+SiO32-+2H2O═H2SiO3↓+2HCO3-
CO2+SiO32-+H2O═H2SiO3↓+CO32-或2CO2+SiO32-+2H2O═H2SiO3↓+2HCO3-
.分析:(1)验证同周期元素金属性强弱的规律,最好选用第3周期的钠、镁、铝三种元素.因为与第2、4、5、6周期相比较,第3周期元素的变化规律较典型;
(2)根据非金属性越强,其最高价氧化物对应水化物的酸性越强,选择对应的酸.
(2)根据非金属性越强,其最高价氧化物对应水化物的酸性越强,选择对应的酸.
解答:解:(1)验证同周期元素金属性强弱的规律,最好选用第三周期的钠、镁、铝三种元素.因为与第2、4、5、6周期相比较,第三周期元素的变化规律较典型;三种金属中钠最活泼,遇水就剧烈反应,与盐酸反应更剧烈,产生大量热,放出H2,可能会着火或爆炸,铝金属活动性最弱,与酸反应比镁要缓慢,但也能产生大量气泡,镁与酸剧烈反应,产生大量气泡;
故答案为:三;钠、镁、铝;①钠剧烈反应,可能着火或爆炸;②镁反应较剧烈,产生大量气泡;③铝反应比镁缓慢,有较多的气泡产生;
(2)乙同学的实验是利用强酸制弱酸的原理.非金属性越强,其最高价氧化物对应水化物的酸性越强.由题意可推测,A为HNO3,B为CaCO3,C为Na2SiO3或K2SiO3;烧杯中二氧化碳与硅酸钠反应生成硅酸沉淀,其反应离子方程式为:CO2+SiO32-+H2O═H2SiO3↓+CO32-或2CO2+SiO32-+2H2O═H2SiO3↓+2HCO3-,
故答案为:①HNO3;CaCO3;Na2SiO3(或K2SiO3);
②CO2+SiO32-+H2O═H2SiO3↓+CO32-或2CO2+SiO32-+2H2O═H2SiO3↓+2HCO3-.
故答案为:三;钠、镁、铝;①钠剧烈反应,可能着火或爆炸;②镁反应较剧烈,产生大量气泡;③铝反应比镁缓慢,有较多的气泡产生;
(2)乙同学的实验是利用强酸制弱酸的原理.非金属性越强,其最高价氧化物对应水化物的酸性越强.由题意可推测,A为HNO3,B为CaCO3,C为Na2SiO3或K2SiO3;烧杯中二氧化碳与硅酸钠反应生成硅酸沉淀,其反应离子方程式为:CO2+SiO32-+H2O═H2SiO3↓+CO32-或2CO2+SiO32-+2H2O═H2SiO3↓+2HCO3-,
故答案为:①HNO3;CaCO3;Na2SiO3(或K2SiO3);
②CO2+SiO32-+H2O═H2SiO3↓+CO32-或2CO2+SiO32-+2H2O═H2SiO3↓+2HCO3-.
点评:本题将元素及其化合物、元素周期律与实验知识结合起来,考查了审题能力、思维能力,具有较强的综合性,有一定的难度.

练习册系列答案
相关题目